검색결과
-
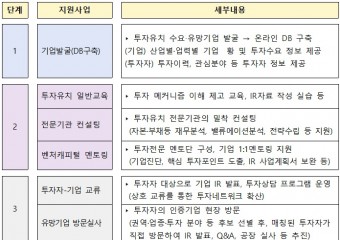
 국표원, 6월부터 샛별(NOVA) 프로젝트 시행국가기술표준원(원장 진종욱, 이하 국표원)에 따르면 6월 부터 본격적으로 '샛별(NOVA) 프로젝트'를 추진한다. 국표원이 추진하는 샛별 프로젝트는 신기술(NET)‧신제품(NEP) 인증기업이 연구개발이나 설비확충에 필요한 투자자금 유치를 지원하는 프로그램이다. 이 사업은 신기술·신제품 인증기업 중 투자유치를 희망하는 기업과 벤처캐피털 등 투자기관의 연결을 지원하는 프로젝트다. 신기술·신제품 인증기업이 성장(scale-up)하기 위해서는 투자자금의 확보가 절실하다. 따라서 국표원은 정부 지원이 필요하다는 현장의 목소리를 반영하여 시행하게 됐다. 소재부품장비투자기관협의회 등과 함께 ▲신기술인증이나 신제품인증을 받은 인증기업들 중 투자유망 기업을 발굴한 후 인증기업과 투자기관의 데이터베이스를 구축해 상호 정보를 탐색할 수 있도록 한다. 또한 ▲투자기관에서 인증기업에게 투자유치를 위한 교육, 컨설팅 등을 제공해 인증기업의 투자유치 역량을 강화할 예정이다. 뿐만아니라 ▲투자설명회(IR), 현장실사 등 투자과정을 거쳐 투자협약, 투자연계형 연구개발(R&D) 등으로 이어지도록 함으로써 가시적인 성과를 이끌어 낼 예정이다. 국표원은 투자유치 지원 프로젝트의 첫 단계로 5월 16일(목요일) 서울시 강남구 섬유센터에서 인증기업들을 대상으로 사업설명회를 개최해 투자유치 지원 프로그램을 안내하고 투자유치 교육도 병행할 계획이다. 참고로 사업설명회는 14:00~15:30까지 섬유센터 2층 컨퍼런스홀(C1)에서 국표원, 소재부품장비투자기관협의회(KITIA), NEP인증협회, 신기술(NET)신제품‧(NEP)인증기업 등이 참석해 진행된다. 진종욱 국가기술표준원장은 “우수한 기술을 가진 신기술‧신제품 인증기업들이 금번 투자유치 지원 프로그램을 통해 중소‧내수기업에서 중견‧수출기업으로 성장하기를 기대하며, 앞으로도 해외마케팅, 금융지원 등 인증기업에 대한 지원 사업을 지속적으로 확대해 나가겠다”고 밝혔다.
국표원, 6월부터 샛별(NOVA) 프로젝트 시행국가기술표준원(원장 진종욱, 이하 국표원)에 따르면 6월 부터 본격적으로 '샛별(NOVA) 프로젝트'를 추진한다. 국표원이 추진하는 샛별 프로젝트는 신기술(NET)‧신제품(NEP) 인증기업이 연구개발이나 설비확충에 필요한 투자자금 유치를 지원하는 프로그램이다. 이 사업은 신기술·신제품 인증기업 중 투자유치를 희망하는 기업과 벤처캐피털 등 투자기관의 연결을 지원하는 프로젝트다. 신기술·신제품 인증기업이 성장(scale-up)하기 위해서는 투자자금의 확보가 절실하다. 따라서 국표원은 정부 지원이 필요하다는 현장의 목소리를 반영하여 시행하게 됐다. 소재부품장비투자기관협의회 등과 함께 ▲신기술인증이나 신제품인증을 받은 인증기업들 중 투자유망 기업을 발굴한 후 인증기업과 투자기관의 데이터베이스를 구축해 상호 정보를 탐색할 수 있도록 한다. 또한 ▲투자기관에서 인증기업에게 투자유치를 위한 교육, 컨설팅 등을 제공해 인증기업의 투자유치 역량을 강화할 예정이다. 뿐만아니라 ▲투자설명회(IR), 현장실사 등 투자과정을 거쳐 투자협약, 투자연계형 연구개발(R&D) 등으로 이어지도록 함으로써 가시적인 성과를 이끌어 낼 예정이다. 국표원은 투자유치 지원 프로젝트의 첫 단계로 5월 16일(목요일) 서울시 강남구 섬유센터에서 인증기업들을 대상으로 사업설명회를 개최해 투자유치 지원 프로그램을 안내하고 투자유치 교육도 병행할 계획이다. 참고로 사업설명회는 14:00~15:30까지 섬유센터 2층 컨퍼런스홀(C1)에서 국표원, 소재부품장비투자기관협의회(KITIA), NEP인증협회, 신기술(NET)신제품‧(NEP)인증기업 등이 참석해 진행된다. 진종욱 국가기술표준원장은 “우수한 기술을 가진 신기술‧신제품 인증기업들이 금번 투자유치 지원 프로그램을 통해 중소‧내수기업에서 중견‧수출기업으로 성장하기를 기대하며, 앞으로도 해외마케팅, 금융지원 등 인증기업에 대한 지원 사업을 지속적으로 확대해 나가겠다”고 밝혔다. -
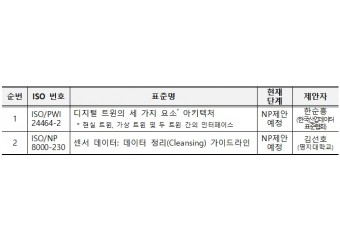
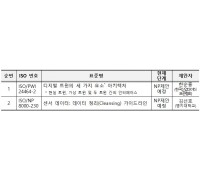 한국, 현실과 가상 공간을 연결하는 디지털 트윈 국제표준 논의 주도산업통상자원부 국가기술표준원(원장 진종욱, 이하 국표원)에 따르면 5월12일~5월17일까지 6일간 ‘산업데이터 국제표준화 회의(ISO TC184 SC4)’가 서울 더케이호텔에서 개최되고 있다. 이번에 개최되는 산업데이터 국제표준화 회의는 국제표준화기구(ISO) 기술위원회(TC) 184 분과위원회(SC)4의 87차 회의로 제조업의 디지털 전환에 관한 국제표준은 논의한다. 디지털 트윈 데이터 관리, 산업 데이터 교환 방식 및 데이터 품질 등에 대한 표준화를 논의하기 위해 한국을 비롯해 미국, 독일, 일본 등 14개 제조 선도국 전문가 50여 명이 참석했다. 조선, 플랜트 등 다양한 산업의 제조 데이터는 IT가 결합된 공장 자동화의 의미를 넘어 스스로 판단하고 조정하는 자율제조에 활용되는 등 산업 디지털 대전환의 핵심 기반이 된다. 이번 회의에서 한국은 △디지털 트윈의 구성요소인 제조 장비·공정 등의 현실트윈 △현실트윈을 디지털로 구현한 가상트윈 △두 트윈을 연결하는 인터페이스를 정립하기 위한 신규 표준안 등을 제안한다. 한국은 △가상트윈을 구현하는 기본원리 △구조 △표현방법 등에 대한 국제표준 개발에 집중해 왔다. 이번 표준안은 디지털 트윈의 공통된 개념 정립과 상호운용성 확보에 기여하고, 기업은 해당 표준을 제조 디지털 전환에 활용할 수 있을 것으로 기대된다. 특히 한국은 현실 제조 공정을 가상 공간으로 구현해 제어하는 디지털 트윈(Digital Twin) 국제표준 논의를 주도한다. 오광해 표준정책국장은 “디지털 트윈은 위험성이 있는 작업 현장에서 사람이 직접 작업하는 것을 대체하고 정교한 공정이 필요한 현장에서 제조 완성도를 높이는 등 중요한 역할을 한다”면서, “국표원은 디지털 트윈을 포함한 산업 데이터 분야 국제표준화 활동을 적극 지원하겠다”고 전했다. 참고로 국표원은 5월 14일(화) 코엑스에서 영국, 일본 등 국제회의 참석자와 국내 제조 전문가가 참여하는'스마트제조 국제표준 포럼'을 개최했다. 인공지능(AI), 빅데이터 등이 제조업으로 빠르게 확산하는 상황에서 표준의 역할에 대한 논의가 진행됐다. 산업데이터 분과위원회(ISO TC184 SC4)는 1984년 설립됐으며 산업 시스템 간 데이터 교환을 위한 제품 데이터 모델 표준에 적용된다. 의장 및 간사는 Mr. Kenneth Swope(미국)와 Ms. Dana Tripp(미국)다. 한국, 미국, 일본, 중국, 독일, 프랑스, 영국, 캐나다, 이탈리아, 스위스 등 P멤버는 22개국, O멤버는 12개국으로 구성되어 있다. SC 4 산하 10개의 작업반(WG)과 2개의 공동작업반(JWG) 등에서 △제품 데이터 교환 모델 △데이터 품질 △디지털 트윈 프레임워크 △공정 사양 언어 등 국제표준 801종을 발간하고 있다.
한국, 현실과 가상 공간을 연결하는 디지털 트윈 국제표준 논의 주도산업통상자원부 국가기술표준원(원장 진종욱, 이하 국표원)에 따르면 5월12일~5월17일까지 6일간 ‘산업데이터 국제표준화 회의(ISO TC184 SC4)’가 서울 더케이호텔에서 개최되고 있다. 이번에 개최되는 산업데이터 국제표준화 회의는 국제표준화기구(ISO) 기술위원회(TC) 184 분과위원회(SC)4의 87차 회의로 제조업의 디지털 전환에 관한 국제표준은 논의한다. 디지털 트윈 데이터 관리, 산업 데이터 교환 방식 및 데이터 품질 등에 대한 표준화를 논의하기 위해 한국을 비롯해 미국, 독일, 일본 등 14개 제조 선도국 전문가 50여 명이 참석했다. 조선, 플랜트 등 다양한 산업의 제조 데이터는 IT가 결합된 공장 자동화의 의미를 넘어 스스로 판단하고 조정하는 자율제조에 활용되는 등 산업 디지털 대전환의 핵심 기반이 된다. 이번 회의에서 한국은 △디지털 트윈의 구성요소인 제조 장비·공정 등의 현실트윈 △현실트윈을 디지털로 구현한 가상트윈 △두 트윈을 연결하는 인터페이스를 정립하기 위한 신규 표준안 등을 제안한다. 한국은 △가상트윈을 구현하는 기본원리 △구조 △표현방법 등에 대한 국제표준 개발에 집중해 왔다. 이번 표준안은 디지털 트윈의 공통된 개념 정립과 상호운용성 확보에 기여하고, 기업은 해당 표준을 제조 디지털 전환에 활용할 수 있을 것으로 기대된다. 특히 한국은 현실 제조 공정을 가상 공간으로 구현해 제어하는 디지털 트윈(Digital Twin) 국제표준 논의를 주도한다. 오광해 표준정책국장은 “디지털 트윈은 위험성이 있는 작업 현장에서 사람이 직접 작업하는 것을 대체하고 정교한 공정이 필요한 현장에서 제조 완성도를 높이는 등 중요한 역할을 한다”면서, “국표원은 디지털 트윈을 포함한 산업 데이터 분야 국제표준화 활동을 적극 지원하겠다”고 전했다. 참고로 국표원은 5월 14일(화) 코엑스에서 영국, 일본 등 국제회의 참석자와 국내 제조 전문가가 참여하는'스마트제조 국제표준 포럼'을 개최했다. 인공지능(AI), 빅데이터 등이 제조업으로 빠르게 확산하는 상황에서 표준의 역할에 대한 논의가 진행됐다. 산업데이터 분과위원회(ISO TC184 SC4)는 1984년 설립됐으며 산업 시스템 간 데이터 교환을 위한 제품 데이터 모델 표준에 적용된다. 의장 및 간사는 Mr. Kenneth Swope(미국)와 Ms. Dana Tripp(미국)다. 한국, 미국, 일본, 중국, 독일, 프랑스, 영국, 캐나다, 이탈리아, 스위스 등 P멤버는 22개국, O멤버는 12개국으로 구성되어 있다. SC 4 산하 10개의 작업반(WG)과 2개의 공동작업반(JWG) 등에서 △제품 데이터 교환 모델 △데이터 품질 △디지털 트윈 프레임워크 △공정 사양 언어 등 국제표준 801종을 발간하고 있다. -
![[특집-ISO/IEC JTC 1/SC 17 활동] 35. Result of voting on SR Ballot for ISO/IEC 7811-7(N 7345)](http://stdnews.kr/data/file/news/thumb/thumb-3555379571_4cufp2BH_756bcefa64e6169e58646ad7b061ecbec455fb11_200x180.jpg) [특집-ISO/IEC JTC 1/SC 17 활동] 35. Result of voting on SR Ballot for ISO/IEC 7811-7(N 7345)2023년 12월04일 ISO/IEC 공동기술위원회 산하 분과위원회 SC 17은 'Result of voting on SR ballot for ISO/IEC 7811-7(N 7345)' 문서를 배포했다.ISO/IEC JTC 1/SC 17 카드 및 개인 식별을 위한 보안장치(Cards and security devices for personal identification)는 국제표준화기구(ISO와 국제전기기술위원회(IEC)의 공동 기술 위원회(JTC) ISO/IEC JTC 1의 표준화 분과위원회다.ISO/IEC JTC 1/SC 17의 국제사무국은 영국에 위치한 영국표준협회(BSI)이며 신분증 및 개인 식별 분야 표준을 개발하고 촉진하는 역할을 담당하고 있다.배포된 문서인 'Result of voting on SR ballot for ISO/IEC 7811-7'은 ISO/IEC 7811-7:2018 (Ed 3)(restricted access)와 관련한 투표결과를 포함하고 있다.ISO/IEC 7811-7:2018 (Ed 3)(restricted access)는 Identification cards — Recording technique — Part 7: Magnetic stripe: High coercivity, high density에 관한 것이다.N 7345 문서는 N 7338, N 7339, N 7340, N 7341, N 7342, N 7343, N 7344 문서와 마찬가지로 2023년 7월15일~12월2일 동안 투표가 진행됐다. 기간 내 각 회원국들은 안건에 대해 의사를 표명했다.투표 항목은 △Confirm △Revise/Amend △Withdraw △Abstain lack of consensus △Abstain lack of national expert input △Stabilize △Q.2 △Q.3 △Q.4 △Q.5 △Q.6 등 총 11개다. 구체적인 질문 내용은 다음과 같다.▷ Q.1 Recommended action▷ Q.2 Has this International Standard been adopted or is it intended to be adopted in the future as a national standard or other publication?▷ Q.3 Is the national publication identical to the International Standard or was it modified?▷ Q.4 If this International Standard has not been nationally adopted, is it applied or used in your country without national adoption or are products/processes/services used in your country based on this standard?▷ Q.5 Is this International Standard, or its national adoption, referenced in regulations in your country?▷ Q.6 If the committee decides to revise or amend, do you propose an expert and/or project leader for the development of that project?참고로 11개 항목 중 투표 결과를 살펴보면 △Confirm 12개국 △Revise/Amend 1개국 △Abstain lack of national expert input 22개국 등으로 나타났다.- 이하 생략 -
[특집-ISO/IEC JTC 1/SC 17 활동] 35. Result of voting on SR Ballot for ISO/IEC 7811-7(N 7345)2023년 12월04일 ISO/IEC 공동기술위원회 산하 분과위원회 SC 17은 'Result of voting on SR ballot for ISO/IEC 7811-7(N 7345)' 문서를 배포했다.ISO/IEC JTC 1/SC 17 카드 및 개인 식별을 위한 보안장치(Cards and security devices for personal identification)는 국제표준화기구(ISO와 국제전기기술위원회(IEC)의 공동 기술 위원회(JTC) ISO/IEC JTC 1의 표준화 분과위원회다.ISO/IEC JTC 1/SC 17의 국제사무국은 영국에 위치한 영국표준협회(BSI)이며 신분증 및 개인 식별 분야 표준을 개발하고 촉진하는 역할을 담당하고 있다.배포된 문서인 'Result of voting on SR ballot for ISO/IEC 7811-7'은 ISO/IEC 7811-7:2018 (Ed 3)(restricted access)와 관련한 투표결과를 포함하고 있다.ISO/IEC 7811-7:2018 (Ed 3)(restricted access)는 Identification cards — Recording technique — Part 7: Magnetic stripe: High coercivity, high density에 관한 것이다.N 7345 문서는 N 7338, N 7339, N 7340, N 7341, N 7342, N 7343, N 7344 문서와 마찬가지로 2023년 7월15일~12월2일 동안 투표가 진행됐다. 기간 내 각 회원국들은 안건에 대해 의사를 표명했다.투표 항목은 △Confirm △Revise/Amend △Withdraw △Abstain lack of consensus △Abstain lack of national expert input △Stabilize △Q.2 △Q.3 △Q.4 △Q.5 △Q.6 등 총 11개다. 구체적인 질문 내용은 다음과 같다.▷ Q.1 Recommended action▷ Q.2 Has this International Standard been adopted or is it intended to be adopted in the future as a national standard or other publication?▷ Q.3 Is the national publication identical to the International Standard or was it modified?▷ Q.4 If this International Standard has not been nationally adopted, is it applied or used in your country without national adoption or are products/processes/services used in your country based on this standard?▷ Q.5 Is this International Standard, or its national adoption, referenced in regulations in your country?▷ Q.6 If the committee decides to revise or amend, do you propose an expert and/or project leader for the development of that project?참고로 11개 항목 중 투표 결과를 살펴보면 △Confirm 12개국 △Revise/Amend 1개국 △Abstain lack of national expert input 22개국 등으로 나타났다.- 이하 생략 - -
![[특집-ISO/IEC JTC 1/SC 17 활동] 34. Result of voting on SR ballot for ISO/IEC 7811-6(N 7344)](http://stdnews.kr/data/file/news/thumb/thumb-3555380113_kIQxAlfN_727cc6e35ccb9d5e6c07574a3b3a2ab9db104d48_200x180.jpg) [특집-ISO/IEC JTC 1/SC 17 활동] 34. Result of voting on SR ballot for ISO/IEC 7811-6(N 7344)2023년 12월04일 ISO/IEC 공동기술위원회 산하 분과위원회 SC 17은 'Result of voting on SR ballot for ISO/IEC 7811-6(N 7344)' 문서를 배포했다.ISO/IEC JTC 1/SC 17 카드 및 개인 식별을 위한 보안장치(Cards and security devices for personal identification)는 국제표준화기구(ISO와 국제전기기술위원회(IEC)의 공동 기술 위원회(JTC) ISO/IEC JTC 1의 표준화 분과위원회다.ISO/IEC JTC 1/SC 17의 국제사무국은 영국에 위치한 영국표준협회(BSI)이며 신분증 및 개인 식별 분야 표준을 개발하고 촉진하는 역할을 담당하고 있다.배포된 문서인 'Result of voting on SR ballot for ISO/IEC 7811-6'은 ISO/IEC 7811-6:2018 (Ed 5)(restricted access)와 관련한 투표결과를 포함하고 있다.ISO/IEC 7811-6:2018 (Ed 5)(restricted access)는 Identification cards — Recording technique — Part 6: Magnetic stripe: High coercivity에 관한 것이다.N 7344 문서는 N 7338, N 7339, N 7340, N 7341, N 7342, N 7343 문서와 마찬가지로 2023년 7월15일~12월2일 동안 투표가 진행됐다. 기간 내 각 회원국들은 안건에 대해 의사를 표명했다.투표 항목은 △Confirm △Revise/Amend △Withdraw △Abstain lack of consensus △Abstain lack of national expert input △Stabilize △Q.2 △Q.3 △Q.4 △Q.5 △Q.6 등 총 11개다. 구체적인 질문 내용은 다음과 같다.▷ Q.1 Recommended action▷ Q.2 Has this International Standard been adopted or is it intended to be adopted in the future as a national standard or other publication?▷ Q.3 Is the national publication identical to the International Standard or was it modified?▷ Q.4 If this International Standard has not been nationally adopted, is it applied or used in your country without national adoption or are products/processes/services used in your country based on this standard?▷ Q.5 Is this International Standard, or its national adoption, referenced in regulations in your country?▷ Q.6 If the committee decides to revise or amend, do you propose an expert and/or project leader for the development of that project?참고로 11개 항목 중 투표 결과를 살펴보면 △Confirm 11개국 △Revise/Amend 1개국 △Abstain lack of national expert input 23개국 등으로 나타났다.- 이하 생략 -
[특집-ISO/IEC JTC 1/SC 17 활동] 34. Result of voting on SR ballot for ISO/IEC 7811-6(N 7344)2023년 12월04일 ISO/IEC 공동기술위원회 산하 분과위원회 SC 17은 'Result of voting on SR ballot for ISO/IEC 7811-6(N 7344)' 문서를 배포했다.ISO/IEC JTC 1/SC 17 카드 및 개인 식별을 위한 보안장치(Cards and security devices for personal identification)는 국제표준화기구(ISO와 국제전기기술위원회(IEC)의 공동 기술 위원회(JTC) ISO/IEC JTC 1의 표준화 분과위원회다.ISO/IEC JTC 1/SC 17의 국제사무국은 영국에 위치한 영국표준협회(BSI)이며 신분증 및 개인 식별 분야 표준을 개발하고 촉진하는 역할을 담당하고 있다.배포된 문서인 'Result of voting on SR ballot for ISO/IEC 7811-6'은 ISO/IEC 7811-6:2018 (Ed 5)(restricted access)와 관련한 투표결과를 포함하고 있다.ISO/IEC 7811-6:2018 (Ed 5)(restricted access)는 Identification cards — Recording technique — Part 6: Magnetic stripe: High coercivity에 관한 것이다.N 7344 문서는 N 7338, N 7339, N 7340, N 7341, N 7342, N 7343 문서와 마찬가지로 2023년 7월15일~12월2일 동안 투표가 진행됐다. 기간 내 각 회원국들은 안건에 대해 의사를 표명했다.투표 항목은 △Confirm △Revise/Amend △Withdraw △Abstain lack of consensus △Abstain lack of national expert input △Stabilize △Q.2 △Q.3 △Q.4 △Q.5 △Q.6 등 총 11개다. 구체적인 질문 내용은 다음과 같다.▷ Q.1 Recommended action▷ Q.2 Has this International Standard been adopted or is it intended to be adopted in the future as a national standard or other publication?▷ Q.3 Is the national publication identical to the International Standard or was it modified?▷ Q.4 If this International Standard has not been nationally adopted, is it applied or used in your country without national adoption or are products/processes/services used in your country based on this standard?▷ Q.5 Is this International Standard, or its national adoption, referenced in regulations in your country?▷ Q.6 If the committee decides to revise or amend, do you propose an expert and/or project leader for the development of that project?참고로 11개 항목 중 투표 결과를 살펴보면 △Confirm 11개국 △Revise/Amend 1개국 △Abstain lack of national expert input 23개국 등으로 나타났다.- 이하 생략 - -
![[특집-ISO/IEC JTC 1/SC 17 활동] 33. Result of voting on SR ballot for ISO/IEC 7811-2(N 7343)](http://stdnews.kr/data/file/news/thumb/thumb-32068165_R52GPIij_2bca2660198a937d2534db7bfd9fc8174a76cfa2_200x180.jpg) [특집-ISO/IEC JTC 1/SC 17 활동] 33. Result of voting on SR ballot for ISO/IEC 7811-2(N 7343)2023년 12월04일 ISO/IEC 공동기술위원회 산하 분과위원회 SC 17은 'Result of voting on SR ballot for ISO/IEC 7811-2(N 7343)' 문서를 배포했다.ISO/IEC JTC 1/SC 17 카드 및 개인 식별을 위한 보안장치(Cards and security devices for personal identification)는 국제표준화기구(ISO와 국제전기기술위원회(IEC)의 공동 기술 위원회(JTC) ISO/IEC JTC 1의 표준화 분과위원회다.ISO/IEC JTC 1/SC 17의 국제사무국은 영국에 위치한 영국표준협회(BSI)이며 신분증 및 개인 식별 분야 표준을 개발하고 촉진하는 역할을 담당하고 있다.배포된 문서인 'Result of voting on SR ballot for ISO/IEC 7811-2'는 ISO/IEC 7811-2:2018 (Ed 5)(restricted access)와 관련한 투표결과를 포함하고 있다. ISO/IEC 7811-2:2018 (Ed 5)(restricted access)는 Identification cards — Recording technique — Part 2: Magnetic stripe: Low coercivity에 관한 것이다. N 7343 문서는 N 7338, N 7339, N 7340, N 7341, N 7342 문서와 마찬가지로 2023년 7월15일~12월2일 동안 투표가 진행됐다. 기간 내 각 회원국들은 안건에 대해 의사를 표명했다.투표 항목은 △Confirm △Revise/Amend △Withdraw △Abstain lack of consensus △Abstain lack of national expert input △Stabilize △Q.2 △Q.3 △Q.4 △Q.5 △Q.6 등 총 11개다. 구체적인 질문 내용은 다음과 같다.▷ Q.1 Recommended action▷ Q.2 Has this International Standard been adopted or is it intended to be adopted in the future as a national standard or other publication?▷ Q.3 Is the national publication identical to the International Standard or was it modified?▷ Q.4 If this International Standard has not been nationally adopted, is it applied or used in your country without national adoption or are products/processes/services used in your country based on this standard?▷ Q.5 Is this International Standard, or its national adoption, referenced in regulations in your country?▷ Q.6 If the committee decides to revise or amend, do you propose an expert and/or project leader for the development of that project?참고로 11개 항목 중 투표 결과를 살펴보면 △Confirm 12개국 △Revise/Amend 1개국 △Abstain lack of consensus 1개국 △Abstain lack of national expert input 21개국 등으로 나타났다. - 이하 생략 -
[특집-ISO/IEC JTC 1/SC 17 활동] 33. Result of voting on SR ballot for ISO/IEC 7811-2(N 7343)2023년 12월04일 ISO/IEC 공동기술위원회 산하 분과위원회 SC 17은 'Result of voting on SR ballot for ISO/IEC 7811-2(N 7343)' 문서를 배포했다.ISO/IEC JTC 1/SC 17 카드 및 개인 식별을 위한 보안장치(Cards and security devices for personal identification)는 국제표준화기구(ISO와 국제전기기술위원회(IEC)의 공동 기술 위원회(JTC) ISO/IEC JTC 1의 표준화 분과위원회다.ISO/IEC JTC 1/SC 17의 국제사무국은 영국에 위치한 영국표준협회(BSI)이며 신분증 및 개인 식별 분야 표준을 개발하고 촉진하는 역할을 담당하고 있다.배포된 문서인 'Result of voting on SR ballot for ISO/IEC 7811-2'는 ISO/IEC 7811-2:2018 (Ed 5)(restricted access)와 관련한 투표결과를 포함하고 있다. ISO/IEC 7811-2:2018 (Ed 5)(restricted access)는 Identification cards — Recording technique — Part 2: Magnetic stripe: Low coercivity에 관한 것이다. N 7343 문서는 N 7338, N 7339, N 7340, N 7341, N 7342 문서와 마찬가지로 2023년 7월15일~12월2일 동안 투표가 진행됐다. 기간 내 각 회원국들은 안건에 대해 의사를 표명했다.투표 항목은 △Confirm △Revise/Amend △Withdraw △Abstain lack of consensus △Abstain lack of national expert input △Stabilize △Q.2 △Q.3 △Q.4 △Q.5 △Q.6 등 총 11개다. 구체적인 질문 내용은 다음과 같다.▷ Q.1 Recommended action▷ Q.2 Has this International Standard been adopted or is it intended to be adopted in the future as a national standard or other publication?▷ Q.3 Is the national publication identical to the International Standard or was it modified?▷ Q.4 If this International Standard has not been nationally adopted, is it applied or used in your country without national adoption or are products/processes/services used in your country based on this standard?▷ Q.5 Is this International Standard, or its national adoption, referenced in regulations in your country?▷ Q.6 If the committee decides to revise or amend, do you propose an expert and/or project leader for the development of that project?참고로 11개 항목 중 투표 결과를 살펴보면 △Confirm 12개국 △Revise/Amend 1개국 △Abstain lack of consensus 1개국 △Abstain lack of national expert input 21개국 등으로 나타났다. - 이하 생략 - -
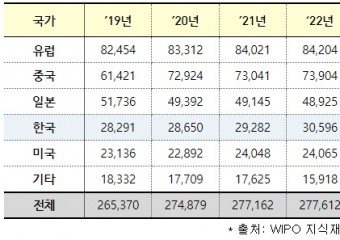
 TTA, 양자 분야 글로벌 표준화 선도한국정보통신기술협회(회장 손승현, 이하 TTA)에 따르면 지난 4월 14일(일요일) 세계 양자의 날(World Quantum Day)을 맞이해 '양자 기술 분야 국제표준화 기구 대응 및 한국 주도 사실표준화 기구 신설을 통한 글로벌 양자기술 국제표준화 선도' 의지를 표명했다. 양자 기술에 대한 국제표준화는 ITU, ETSI, IRTF 등에서 세부 기술 분야별로 추진되었으나, 최근 신설된 ISO와 IEC의 합동기술위원회인 JTC 3(양자기술, 의장국: 한국)를 중심으로 본격적으로 진행될 것으로 예상되기 때문이다. TTA는 지난 20여 년간 국내 산·학·연의 국제표준화 활동지원 프로그램을 운영하고 있는 ICT 표준화 전문기관이다. 따라서 양자통신, 양자암호 등 관련 전문가 10여 명을 확보해 꾸준한 지원을 통해 ITU-T 양자 기술 관련(ITU-T SG11(프로토콜) 3건, SG13(미래 네트워크) 10건, SG17(정보보호) 3건 등) 의장단 3석(27%)을 진출시켰다. 또한 '양자키분배 네트워크 상호연동 보안 요구사항(X.sec_QKDNI)'등 16건(51.6%)이 우리나라 주도로 진행 중이다. 특히, 양자 기술 분야에서 ITU-T 최초의 표준은 우리나라가 제안한 Y.3800(양자키 분배망 개요)*으로 2019년 승인됐다. Y.3800(양자키 분배망 개요)는 ITU-T Y.3800 Overview on networks supporting quantum key distribution이다. 2024년 현재까지 SG11(프로토콜) 5건, SG13(미래 네트워크) 20건, SG17(정보보호) 6건 등 총 31건의 유관 표준이 제정됐다. TTA는 양자기술 시장 표준화 선도 및 양자 ICT 산업화 촉진을 위해 세계 최초로 한국 주도의 '글로벌 사실표준화기구'를 2024년 하반기 출범을 목표로 추진중이다. 양자 분야 글로벌 사실표준화 기수의 명칭은 QINSA(Quantum INformation Standard Association, 이하 QINSA)이며 IBM을 포함해 양자 전문기업 10개가 참여하고, 국내 이동통신 3사(KT, SKT, LGU+) 및 중소기업 등 100여 개 국내외 회원사를 확보했다. QINSA는 작업반(통신, 컴퓨팅, 센서) 통해 표준개발, 유즈케이스·비즈니스 모델을 발굴하며 미국 QED-C, 일본 Q-STAR, 유럽연합 QUIC 등 양자 분야 산업협의체와 다양한 협력을 통해 글로벌 사실표준화기구로서 위상을 제고할 예정이다. TTA 손승현 회장은 '우리나라가 표준을 기반으로 글로벌 시장에서 양자 기술 경쟁력을 강화하고 선도적인 위치를 확보할 수 있도록 양자 기술의 표준화 활동을 지속적으로 확대해 나가겠다'고 밝혔다.
TTA, 양자 분야 글로벌 표준화 선도한국정보통신기술협회(회장 손승현, 이하 TTA)에 따르면 지난 4월 14일(일요일) 세계 양자의 날(World Quantum Day)을 맞이해 '양자 기술 분야 국제표준화 기구 대응 및 한국 주도 사실표준화 기구 신설을 통한 글로벌 양자기술 국제표준화 선도' 의지를 표명했다. 양자 기술에 대한 국제표준화는 ITU, ETSI, IRTF 등에서 세부 기술 분야별로 추진되었으나, 최근 신설된 ISO와 IEC의 합동기술위원회인 JTC 3(양자기술, 의장국: 한국)를 중심으로 본격적으로 진행될 것으로 예상되기 때문이다. TTA는 지난 20여 년간 국내 산·학·연의 국제표준화 활동지원 프로그램을 운영하고 있는 ICT 표준화 전문기관이다. 따라서 양자통신, 양자암호 등 관련 전문가 10여 명을 확보해 꾸준한 지원을 통해 ITU-T 양자 기술 관련(ITU-T SG11(프로토콜) 3건, SG13(미래 네트워크) 10건, SG17(정보보호) 3건 등) 의장단 3석(27%)을 진출시켰다. 또한 '양자키분배 네트워크 상호연동 보안 요구사항(X.sec_QKDNI)'등 16건(51.6%)이 우리나라 주도로 진행 중이다. 특히, 양자 기술 분야에서 ITU-T 최초의 표준은 우리나라가 제안한 Y.3800(양자키 분배망 개요)*으로 2019년 승인됐다. Y.3800(양자키 분배망 개요)는 ITU-T Y.3800 Overview on networks supporting quantum key distribution이다. 2024년 현재까지 SG11(프로토콜) 5건, SG13(미래 네트워크) 20건, SG17(정보보호) 6건 등 총 31건의 유관 표준이 제정됐다. TTA는 양자기술 시장 표준화 선도 및 양자 ICT 산업화 촉진을 위해 세계 최초로 한국 주도의 '글로벌 사실표준화기구'를 2024년 하반기 출범을 목표로 추진중이다. 양자 분야 글로벌 사실표준화 기수의 명칭은 QINSA(Quantum INformation Standard Association, 이하 QINSA)이며 IBM을 포함해 양자 전문기업 10개가 참여하고, 국내 이동통신 3사(KT, SKT, LGU+) 및 중소기업 등 100여 개 국내외 회원사를 확보했다. QINSA는 작업반(통신, 컴퓨팅, 센서) 통해 표준개발, 유즈케이스·비즈니스 모델을 발굴하며 미국 QED-C, 일본 Q-STAR, 유럽연합 QUIC 등 양자 분야 산업협의체와 다양한 협력을 통해 글로벌 사실표준화기구로서 위상을 제고할 예정이다. TTA 손승현 회장은 '우리나라가 표준을 기반으로 글로벌 시장에서 양자 기술 경쟁력을 강화하고 선도적인 위치를 확보할 수 있도록 양자 기술의 표준화 활동을 지속적으로 확대해 나가겠다'고 밝혔다. -
![[특집-기술위원회] TC 215 - 의료 정보학(Health informatics)](http://stdnews.kr/data/file/news/thumb/thumb-32068165_7HDAVCBF_87cd4effcac1b626d770aadf6bb9d9045d64b00f_200x180.jpg) [특집-기술위원회] TC 215 - 의료 정보학(Health informatics)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~107 △1963년 TC 108~111 △1964년 TC 112~115, TC 117 △1965년 TC 118 △1966년 TC 119~122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146~150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~161 △1975년 TC 162~164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171~174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~186 △1984년 TC 188 △1985년 TC 189~191 △1988년 TC 192~194 △1989년 TC 195 △1990년 TC 197, TC 198 △1991년 TC 199, TC 201, TC 202 △1992년 TC 204~206 △1993년 TC 209 △1994년 TC 210, TC 211 △1996년 TC 213, TC 214 등이 있다.ISO/TC 215 의료 정보학(Health informatics)과 관련된 기술위원회는 1998년 결성됐다. 사무국은 미국 표준협회(American National Standards Institute, ANSI)에서 맡고 있다.위원회는 레이첼 호손(Ms Rachel Hawthorne)가 책임지고 있다. 현재 의장은 토드 쿠퍼(Mr Todd Cooper)이며 임기는 2026년 말까지다. ISO 기술 프로그램 관리자는 마호 다카하시(Mme Maho Takahashi), ISO 편집 관리자는 발레리아 아가넨노네(Ms Valeria Agamennone) 등이다.범위는 의료 관련 데이터, 의료 시스템의 모든 측면을 지원하고 활성화하는 지식의 수집, 교환 및 사용을 촉진하기 위한 의료 정보학 분야의 표준화다.현재 ISO/TC 215 사무국과 관련해 발행된 표준은 237개며 ISO/TC 215 사무국의 직접적인 책임 하에 발행된 표준은 225개다.ISO/TC 215과 관련해 개발 중인 표준은 64개며 이중 ISO/TC 215 사무국의 직접적인 책임 하에 개발 중인 표준은 62개다. 참여하고 있는 회원은 35개국, 참관 회원은 32개국이다.□ ISO/TC 215 사무국의 직접적인 책임 하에 발행된 표준 225개 중 15개 목록▷ISO 1828:2012 Health informatics — Categorial structure for terminological systems of surgical procedures▷ISO/TR 4421:2023 Health informatics — Introduction to Ayurveda informatics▷ISO/TS 5044:2023 Health informatics — Information model for quality control of traditional Chinese medicinal products▷ISO/TS 5118:2022 Health informatics — Categorial structure of representation for evaluation of clinical practice guidelines of traditional Chinese medicine▷ISO/TS 5346:2022 Health informatics — Categorial structure for representation of traditional Chinese medicine clinical decision support system▷ISO 5477:2023 Health informatics — Interoperability of public health emergency preparedness and response information systems▷ISO/TS 5499:2024 Health informatics — Clinical particulars — Core principles for the harmonization of therapeutic indications terms and identifiers▷ISO/TS 5568:2022 Health informatics — Traditional Chinese medicine — Labelling metadata of human biological sample information▷ISO/TS 5569:2023 Health informatics — Conceptual data model for Chinese medicinal herbs▷ISO/TR 9143:2023 Health informatics — Sex and gender in electronic health records▷ISO 10159:2011 Health informatics — Messages and communication — Web access reference manifest▷ISO 10781:2023 Health informatics — HL7 Electronic Health Record-System Functional Model, Release 2.1 (EHR FM)▷ISO/IEEE 11073-00103:2015 Health informatics — Personal health device communication — Part 00103: Overview▷ISO/IEEE 11073-10101:2020 Health informatics — Device interoperability — Part 10101: Point-of-care medical device communication — Nomenclature▷ISO/IEEE 11073-10102:2014 Health informatics — Point-of-care medical device communication — Part 10102: Nomenclature — Annotated ECG□ ISO/TC 215 사무국의 직접적인 책임 하에 개발 중인 표준 62개 중 15개 목록▷ISO/AWI TR 4419 Health informatics — Reducing clinicians burden▷ISO/DTS 5384 Health informatics - Categorial Structure and Data Elements for the Identification and Exchange of Immunization Data▷ISO/CD TS 5615 Health informatics — Accelerating Safe, Effective and Secure Remote Connected Care and Mobile Health Through Standards-Based Interoperability Solutions Addressing Gaps Revealed by Pandemics▷ISO/DTS 5777 Health informatics — The architecture of internet healthcare service network▷ISO/DTS 5788 Health informatics — Internet healthcare service pattern▷ISO/CD TS 6201.2 Health Informatics — Personalized Digital Health -Framework▷ISO/CD TS 6204 Health Informatics — Categorial structures for representation of Ayurvedic medicinal water — Decocting process in Ayurveda▷ISO/AWI TS 6226 Health informatics — Reference architecture for syndromic surveillance systems for infectious diseases▷ISO/DTR 6231 Health informatics — Standardizing graphical content▷ISO/CD TS 6268-1 Health informatics — Cybersecurity framework for telehealth environments — Part 1: Overview and Concepts▷ISO/AWI TS 6268-2 Health informatics — Cybersecurity framework for telehealth environments — Part 2: Cybersecurity reference models of telehealth▷ISO/CD TS 7122 Health Informatics — Guidelines for exchanging data generated by POCT (Point of Care Testing) devices between screening center and clinical laboratory▷ISO/AWI TS 9166 Health Informatics — Guidelines for self-assessment questionnaire systems▷ISO/DTS 9320 Health informatics — Standardized data set for transfer of hemodialysis patients▷ISO/DTS 9321 Health informatics — General requirements of multi-centre medical data collaborative analysis□ ISO/TC 215 사무국 분과위원회(Subcommittee)의 책임 하에 발행 및 개발 중인 표준 현황▷ISO/TC 215/SC 1 Genomics Informatics ; 발행된 표준 12개, 개발 중인 표준 2개
[특집-기술위원회] TC 215 - 의료 정보학(Health informatics)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~107 △1963년 TC 108~111 △1964년 TC 112~115, TC 117 △1965년 TC 118 △1966년 TC 119~122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146~150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~161 △1975년 TC 162~164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171~174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~186 △1984년 TC 188 △1985년 TC 189~191 △1988년 TC 192~194 △1989년 TC 195 △1990년 TC 197, TC 198 △1991년 TC 199, TC 201, TC 202 △1992년 TC 204~206 △1993년 TC 209 △1994년 TC 210, TC 211 △1996년 TC 213, TC 214 등이 있다.ISO/TC 215 의료 정보학(Health informatics)과 관련된 기술위원회는 1998년 결성됐다. 사무국은 미국 표준협회(American National Standards Institute, ANSI)에서 맡고 있다.위원회는 레이첼 호손(Ms Rachel Hawthorne)가 책임지고 있다. 현재 의장은 토드 쿠퍼(Mr Todd Cooper)이며 임기는 2026년 말까지다. ISO 기술 프로그램 관리자는 마호 다카하시(Mme Maho Takahashi), ISO 편집 관리자는 발레리아 아가넨노네(Ms Valeria Agamennone) 등이다.범위는 의료 관련 데이터, 의료 시스템의 모든 측면을 지원하고 활성화하는 지식의 수집, 교환 및 사용을 촉진하기 위한 의료 정보학 분야의 표준화다.현재 ISO/TC 215 사무국과 관련해 발행된 표준은 237개며 ISO/TC 215 사무국의 직접적인 책임 하에 발행된 표준은 225개다.ISO/TC 215과 관련해 개발 중인 표준은 64개며 이중 ISO/TC 215 사무국의 직접적인 책임 하에 개발 중인 표준은 62개다. 참여하고 있는 회원은 35개국, 참관 회원은 32개국이다.□ ISO/TC 215 사무국의 직접적인 책임 하에 발행된 표준 225개 중 15개 목록▷ISO 1828:2012 Health informatics — Categorial structure for terminological systems of surgical procedures▷ISO/TR 4421:2023 Health informatics — Introduction to Ayurveda informatics▷ISO/TS 5044:2023 Health informatics — Information model for quality control of traditional Chinese medicinal products▷ISO/TS 5118:2022 Health informatics — Categorial structure of representation for evaluation of clinical practice guidelines of traditional Chinese medicine▷ISO/TS 5346:2022 Health informatics — Categorial structure for representation of traditional Chinese medicine clinical decision support system▷ISO 5477:2023 Health informatics — Interoperability of public health emergency preparedness and response information systems▷ISO/TS 5499:2024 Health informatics — Clinical particulars — Core principles for the harmonization of therapeutic indications terms and identifiers▷ISO/TS 5568:2022 Health informatics — Traditional Chinese medicine — Labelling metadata of human biological sample information▷ISO/TS 5569:2023 Health informatics — Conceptual data model for Chinese medicinal herbs▷ISO/TR 9143:2023 Health informatics — Sex and gender in electronic health records▷ISO 10159:2011 Health informatics — Messages and communication — Web access reference manifest▷ISO 10781:2023 Health informatics — HL7 Electronic Health Record-System Functional Model, Release 2.1 (EHR FM)▷ISO/IEEE 11073-00103:2015 Health informatics — Personal health device communication — Part 00103: Overview▷ISO/IEEE 11073-10101:2020 Health informatics — Device interoperability — Part 10101: Point-of-care medical device communication — Nomenclature▷ISO/IEEE 11073-10102:2014 Health informatics — Point-of-care medical device communication — Part 10102: Nomenclature — Annotated ECG□ ISO/TC 215 사무국의 직접적인 책임 하에 개발 중인 표준 62개 중 15개 목록▷ISO/AWI TR 4419 Health informatics — Reducing clinicians burden▷ISO/DTS 5384 Health informatics - Categorial Structure and Data Elements for the Identification and Exchange of Immunization Data▷ISO/CD TS 5615 Health informatics — Accelerating Safe, Effective and Secure Remote Connected Care and Mobile Health Through Standards-Based Interoperability Solutions Addressing Gaps Revealed by Pandemics▷ISO/DTS 5777 Health informatics — The architecture of internet healthcare service network▷ISO/DTS 5788 Health informatics — Internet healthcare service pattern▷ISO/CD TS 6201.2 Health Informatics — Personalized Digital Health -Framework▷ISO/CD TS 6204 Health Informatics — Categorial structures for representation of Ayurvedic medicinal water — Decocting process in Ayurveda▷ISO/AWI TS 6226 Health informatics — Reference architecture for syndromic surveillance systems for infectious diseases▷ISO/DTR 6231 Health informatics — Standardizing graphical content▷ISO/CD TS 6268-1 Health informatics — Cybersecurity framework for telehealth environments — Part 1: Overview and Concepts▷ISO/AWI TS 6268-2 Health informatics — Cybersecurity framework for telehealth environments — Part 2: Cybersecurity reference models of telehealth▷ISO/CD TS 7122 Health Informatics — Guidelines for exchanging data generated by POCT (Point of Care Testing) devices between screening center and clinical laboratory▷ISO/AWI TS 9166 Health Informatics — Guidelines for self-assessment questionnaire systems▷ISO/DTS 9320 Health informatics — Standardized data set for transfer of hemodialysis patients▷ISO/DTS 9321 Health informatics — General requirements of multi-centre medical data collaborative analysis□ ISO/TC 215 사무국 분과위원회(Subcommittee)의 책임 하에 발행 및 개발 중인 표준 현황▷ISO/TC 215/SC 1 Genomics Informatics ; 발행된 표준 12개, 개발 중인 표준 2개 -
 KTL, AI 신뢰성 확보와 글로벌 네트워크 강화를 위해 힘쓰다한국산업기술시험원(KTL, 원장 김세종)이 인공지능(AI) 신뢰성 확보와 글로벌 네트워크 강화를 위해 트레인 글로벌(이하 TRAIN)이 주최하는 「제1차 TRAIN 글로벌 심포지엄」에 참가했다고 밝혔다. 이번 심포지엄은 「신뢰할 수 있는 AI를 위한 아시아 연대, 정보 교류의 힘」이라는 주제로 그래비티 서울 판교 오토그래프 컬렉션에서 개최되었다. 더불어 국내외 정부·공공기관, AI 관련 기업·협회·단체를 비롯한 약 150여 명이 참석했다. 이번 행사를 주관한 TRAIN은 Global TRustworthy AI International Network의 약자이며, AI 신뢰성 확보와 기술규제 공동 대응을 위한 국제연대이다. 현재 대한민국, 베트남, 태국, 중국이 창립회원 국가로 소속되어 활동 중이다. 한편, KTL은 AI 접목 제품 및 서비스가 급증함에 따라 해외수출 제품에 대한 AI 신뢰성 검증 수요에 대응하기 위해 산업 디지털 전환 적합성 인증체계 마련과 실증 기반을 2026년까지 충남 아산시에 구축할 계획이라고 밝혔다. 이를 통해 우리 기업들이 국제 무대에서 경쟁력을 가질 수 있도록 지원 활동을 이어갈 예정이다. 또한, 산업통상자원부와 함께 KTL은 국내 AI 공급 기업의 수출 지원을 위해 「산업AI국제인증 포럼」을 발족하여 산업AI 인증체계를 마련하고 있다. 이를 통해 AI 기술개발 단계부터 신뢰성을 확인할 수 있도록 지원 활동을 이어갈 것으로 전망된다.
KTL, AI 신뢰성 확보와 글로벌 네트워크 강화를 위해 힘쓰다한국산업기술시험원(KTL, 원장 김세종)이 인공지능(AI) 신뢰성 확보와 글로벌 네트워크 강화를 위해 트레인 글로벌(이하 TRAIN)이 주최하는 「제1차 TRAIN 글로벌 심포지엄」에 참가했다고 밝혔다. 이번 심포지엄은 「신뢰할 수 있는 AI를 위한 아시아 연대, 정보 교류의 힘」이라는 주제로 그래비티 서울 판교 오토그래프 컬렉션에서 개최되었다. 더불어 국내외 정부·공공기관, AI 관련 기업·협회·단체를 비롯한 약 150여 명이 참석했다. 이번 행사를 주관한 TRAIN은 Global TRustworthy AI International Network의 약자이며, AI 신뢰성 확보와 기술규제 공동 대응을 위한 국제연대이다. 현재 대한민국, 베트남, 태국, 중국이 창립회원 국가로 소속되어 활동 중이다. 한편, KTL은 AI 접목 제품 및 서비스가 급증함에 따라 해외수출 제품에 대한 AI 신뢰성 검증 수요에 대응하기 위해 산업 디지털 전환 적합성 인증체계 마련과 실증 기반을 2026년까지 충남 아산시에 구축할 계획이라고 밝혔다. 이를 통해 우리 기업들이 국제 무대에서 경쟁력을 가질 수 있도록 지원 활동을 이어갈 예정이다. 또한, 산업통상자원부와 함께 KTL은 국내 AI 공급 기업의 수출 지원을 위해 「산업AI국제인증 포럼」을 발족하여 산업AI 인증체계를 마련하고 있다. 이를 통해 AI 기술개발 단계부터 신뢰성을 확인할 수 있도록 지원 활동을 이어갈 것으로 전망된다. -
![[특집-기술위원회] TC 198 - 보건 의료 제품의 멸균(Sterilization of health care products)](http://stdnews.kr/data/file/news/thumb/thumb-32068165_2BoG0P7X_a0e507b4052a7f3b37d893ad86a6c6caa79da3d8_200x180.jpg) [특집-기술위원회] TC 198 - 보건 의료 제품의 멸균(Sterilization of health care products)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~TC 67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~TC 107 △1963년 TC 108~TC 111 △1964년 TC 112~TC 115, TC 117 △1965년 TC 118 △1966년 TC 119~TC 122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146, TC 147, TC 148, TC 149, TC 150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~TC 161 △1975년 TC 162~TC 164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171, TC 172, TC 173, TC 174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~TC 186 △1984년 TC 188 △1985년 TC 189, TC 190, TC 191 △1988년 TC 192~TC 194 △1989년 TC 195 등이 있다.ISO/TC 198 보건 의료 제품의 멸균(Sterilization of health care products)과 관련된 기술위원회는 TC 197과 마찬가지로 1990년 결성됐다. 사무국은 미국 표준협회(American National Standards Institute, ANSI)에서 맡고 있다.위원회는 아만다 베네딕(Ms Amanda Benedict)가 책임지고 있다. 현재 의장은 리차드 밴크로프트(Mr Richard Bancroft)이며 임기는 2025년 말까지다.ISO 기술 프로그램 관리자는 페트리샤 쿡(Mme Patricia Cook), ISO 편집 관리자는 클라우디아 루에제(Ms Claudia Lueje)등이다. 범위는 보건의료 제품의 멸균을 위한 프로세스 및 장비의 표준화다.현재 ISO/TC 198 사무국의 직접적인 책임 하에 발행된 표준은 69개며 ISO/TC 198 사무국의 직접적인 책임 하에 개발 중인 표준은 15개다. 참여하고 있는 회원은 34개국, 참관 회원은 21개국이다.□ ISO/TC 198 사무국의 직접적인 책임 하에 발행된 표준 69개 중 15개 목록▷ISO/TS 5111:2022 Guidance on quality of water for sterilizers, sterilization and washer-disinfectors for health care products▷ISO 11135:2014 Sterilization of health-care products — Ethylene oxide — Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO 11135:2014/Amd 1:2018 Sterilization of health-care products — Ethylene oxide — Requirements for the development, validation and routine control of a sterilization process for medical devices — Amendment 1: Revision of Annex E, Single batch release▷ISO 11137-1:2006 Sterilization of health care products — Radiation — Part 1: Requirements for development, validation and routine control of a sterilization process for medical devices▷ISO 11137-1:2006/Amd 1:2013 Sterilization of health care products — Radiation — Part 1: Requirements for development, validation and routine control of a sterilization process for medical devices — Amendment 1▷ISO 11137-1:2006/Amd 2:2018 Sterilization of health care products — Radiation — Part 1: Requirements for development, validation and routine control of a sterilization process for medical devices — Amendment 2: Revision to 4.3.4 and 11.2▷ISO 11137-2:2013 Sterilization of health care products — Radiation — Part 2: Establishing the sterilization dose▷ISO 11137-2:2013/Amd 1:2022 Sterilization of health care products — Radiation — Part 2: Establishing the sterilization dose — Amendment 1▷ISO 11137-3:2017 Sterilization of health care products — Radiation — Part 3: Guidance on dosimetric aspects of development, validation and routine control▷ISO/TS 11137-4:2020 Sterilization of health care products — Radiation — Part 4: Guidance on process control▷ISO 11138-1:2017 Sterilization of health care products — Biological indicators — Part 1: General requirements▷ISO 11138-2:2017 Sterilization of health care products — Biological indicators — Part 2: Biological indicators for ethylene oxide sterilization processes▷ISO 11138-3:2017 Sterilization of health care products — Biological indicators — Part 3: Biological indicators for moist heat sterilization processes▷ISO 11138-4:2017 Sterilization of health care products — Biological indicators — Part 4: Biological indicators for dry heat sterilization processes▷ISO 11138-5:2017 Sterilization of health care products — Biological indicators — Part 5: Biological indicators for low-temperature steam and formaldehyde sterilization processes□ ISO/TC 198 사무국의 직접적인 책임 하에 개발 중인 표준 15개 목록▷ISO/DIS 11135.2 Sterilization of health care products — Ethylene oxide — Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO/FDIS 11137-1 Sterilization of health care products — Radiation — Part 1: Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO/CD 11140-3 Sterilization of health care products — Chemical indicators — Part 3: Class 2 indicator systems for use in the Bowie and Dick-type steam penetration test▷ISO/CD 11140-4 Sterilization of health care products — Chemical indicators — Part 4: Class 2 indicators as an alternative to the Bowie and Dick-type test for detection of steam penetration▷ISO/CD 11140-5 Sterilization of health care products — Chemical indicators — Part 5: Class 2 indicators for Bowie and Dick-type air removal tests▷ISO/AWI 11607-3 Packaging for terminally sterilized medical devices — Part 3: Requirements for process development for forming, sealing and assembly▷ISO/AWI 11737-1 Sterilization of health care products — Microbiological methods — Part 1: Determination of a population of microorganisms on products▷ISO/FDIS 15883-1 Washer-disinfectors — Part 1: General requirements, terms and definitions and tests▷ISO/DIS 15883-2 Washer-disinfectors — Part 2: Requirements and tests for washer-disinfectors employing thermal disinfection for critical and semi-critical medical devices▷ISO/DIS 15883-3 Washer-disinfectors — Part 3: Requirements and tests for washer-disinfectors employing thermal disinfection for human waste containers▷ISO/CD 15883-6 Washer-disinfectors — Part 6: Requirements and tests for washer-disinfectors employing thermal disinfection for noncritical medical devices and health care equipment▷ISO/DIS 15883-7 Washer-disinfectors — Part 7: Requirements and tests for washer-disinfectors employing chemical disinfection for non-critical thermolabile medical devices and health care equipment▷ISO/AWI TS 17664-3 Processing of health care products — Information to be provided by the medical device manufacturer for the processing of medical devices — Part 3: Guidance on the designation of a reusable medical device to a quantitative cleaning classification▷ISO 17665 Sterilization of health care products — Moist heat — Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO/AWI 19253 Sterilization of health care products — Application of ISO/TS 22421 to the requirements for sterilizers used for the terminal sterilization of health care products containing aqueous liquid in sealed containers
[특집-기술위원회] TC 198 - 보건 의료 제품의 멸균(Sterilization of health care products)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~TC 67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~TC 107 △1963년 TC 108~TC 111 △1964년 TC 112~TC 115, TC 117 △1965년 TC 118 △1966년 TC 119~TC 122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146, TC 147, TC 148, TC 149, TC 150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~TC 161 △1975년 TC 162~TC 164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171, TC 172, TC 173, TC 174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~TC 186 △1984년 TC 188 △1985년 TC 189, TC 190, TC 191 △1988년 TC 192~TC 194 △1989년 TC 195 등이 있다.ISO/TC 198 보건 의료 제품의 멸균(Sterilization of health care products)과 관련된 기술위원회는 TC 197과 마찬가지로 1990년 결성됐다. 사무국은 미국 표준협회(American National Standards Institute, ANSI)에서 맡고 있다.위원회는 아만다 베네딕(Ms Amanda Benedict)가 책임지고 있다. 현재 의장은 리차드 밴크로프트(Mr Richard Bancroft)이며 임기는 2025년 말까지다.ISO 기술 프로그램 관리자는 페트리샤 쿡(Mme Patricia Cook), ISO 편집 관리자는 클라우디아 루에제(Ms Claudia Lueje)등이다. 범위는 보건의료 제품의 멸균을 위한 프로세스 및 장비의 표준화다.현재 ISO/TC 198 사무국의 직접적인 책임 하에 발행된 표준은 69개며 ISO/TC 198 사무국의 직접적인 책임 하에 개발 중인 표준은 15개다. 참여하고 있는 회원은 34개국, 참관 회원은 21개국이다.□ ISO/TC 198 사무국의 직접적인 책임 하에 발행된 표준 69개 중 15개 목록▷ISO/TS 5111:2022 Guidance on quality of water for sterilizers, sterilization and washer-disinfectors for health care products▷ISO 11135:2014 Sterilization of health-care products — Ethylene oxide — Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO 11135:2014/Amd 1:2018 Sterilization of health-care products — Ethylene oxide — Requirements for the development, validation and routine control of a sterilization process for medical devices — Amendment 1: Revision of Annex E, Single batch release▷ISO 11137-1:2006 Sterilization of health care products — Radiation — Part 1: Requirements for development, validation and routine control of a sterilization process for medical devices▷ISO 11137-1:2006/Amd 1:2013 Sterilization of health care products — Radiation — Part 1: Requirements for development, validation and routine control of a sterilization process for medical devices — Amendment 1▷ISO 11137-1:2006/Amd 2:2018 Sterilization of health care products — Radiation — Part 1: Requirements for development, validation and routine control of a sterilization process for medical devices — Amendment 2: Revision to 4.3.4 and 11.2▷ISO 11137-2:2013 Sterilization of health care products — Radiation — Part 2: Establishing the sterilization dose▷ISO 11137-2:2013/Amd 1:2022 Sterilization of health care products — Radiation — Part 2: Establishing the sterilization dose — Amendment 1▷ISO 11137-3:2017 Sterilization of health care products — Radiation — Part 3: Guidance on dosimetric aspects of development, validation and routine control▷ISO/TS 11137-4:2020 Sterilization of health care products — Radiation — Part 4: Guidance on process control▷ISO 11138-1:2017 Sterilization of health care products — Biological indicators — Part 1: General requirements▷ISO 11138-2:2017 Sterilization of health care products — Biological indicators — Part 2: Biological indicators for ethylene oxide sterilization processes▷ISO 11138-3:2017 Sterilization of health care products — Biological indicators — Part 3: Biological indicators for moist heat sterilization processes▷ISO 11138-4:2017 Sterilization of health care products — Biological indicators — Part 4: Biological indicators for dry heat sterilization processes▷ISO 11138-5:2017 Sterilization of health care products — Biological indicators — Part 5: Biological indicators for low-temperature steam and formaldehyde sterilization processes□ ISO/TC 198 사무국의 직접적인 책임 하에 개발 중인 표준 15개 목록▷ISO/DIS 11135.2 Sterilization of health care products — Ethylene oxide — Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO/FDIS 11137-1 Sterilization of health care products — Radiation — Part 1: Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO/CD 11140-3 Sterilization of health care products — Chemical indicators — Part 3: Class 2 indicator systems for use in the Bowie and Dick-type steam penetration test▷ISO/CD 11140-4 Sterilization of health care products — Chemical indicators — Part 4: Class 2 indicators as an alternative to the Bowie and Dick-type test for detection of steam penetration▷ISO/CD 11140-5 Sterilization of health care products — Chemical indicators — Part 5: Class 2 indicators for Bowie and Dick-type air removal tests▷ISO/AWI 11607-3 Packaging for terminally sterilized medical devices — Part 3: Requirements for process development for forming, sealing and assembly▷ISO/AWI 11737-1 Sterilization of health care products — Microbiological methods — Part 1: Determination of a population of microorganisms on products▷ISO/FDIS 15883-1 Washer-disinfectors — Part 1: General requirements, terms and definitions and tests▷ISO/DIS 15883-2 Washer-disinfectors — Part 2: Requirements and tests for washer-disinfectors employing thermal disinfection for critical and semi-critical medical devices▷ISO/DIS 15883-3 Washer-disinfectors — Part 3: Requirements and tests for washer-disinfectors employing thermal disinfection for human waste containers▷ISO/CD 15883-6 Washer-disinfectors — Part 6: Requirements and tests for washer-disinfectors employing thermal disinfection for noncritical medical devices and health care equipment▷ISO/DIS 15883-7 Washer-disinfectors — Part 7: Requirements and tests for washer-disinfectors employing chemical disinfection for non-critical thermolabile medical devices and health care equipment▷ISO/AWI TS 17664-3 Processing of health care products — Information to be provided by the medical device manufacturer for the processing of medical devices — Part 3: Guidance on the designation of a reusable medical device to a quantitative cleaning classification▷ISO 17665 Sterilization of health care products — Moist heat — Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO/AWI 19253 Sterilization of health care products — Application of ISO/TS 22421 to the requirements for sterilizers used for the terminal sterilization of health care products containing aqueous liquid in sealed containers -
![[특집-기술위원회] TC 194 - 의료 장비의 생물학적 및 임상적 평가(Biological and clinical evaluation of medical devices)](http://stdnews.kr/data/file/news/thumb/thumb-3743812600_FrLCzJ0v_6a77c2077882a93f0804dbd4f16e6e8eefd439e0_200x180.jpg) [특집-기술위원회] TC 194 - 의료 장비의 생물학적 및 임상적 평가(Biological and clinical evaluation of medical devices)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~TC 67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~TC 107 △1963년 TC 108~TC 111 △1964년 TC 112~TC 115, TC 117 △1965년 TC 118 △1966년 TC 119~TC 122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146, TC 147, TC 148, TC 149, TC 150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~TC 161 △1975년 TC 162~TC 164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171, TC 172, TC 173, TC 174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~TC 186 △1984년 TC 188 △1985년 TC 189, TC 190, TC 191 등이 있다.ISO/TC 194 의료 장비의 생물학적 및 임상적 평가(Biological and clinical evaluation of medical devices)와 관련된 기술위원회는 TC 192, TC 193과 마찬가지로 1988년 결성됐다. 사무국은 독일 표준화기구(Deutsches Institut für Normung e.V., DIN)에서 맡고 있다.위원회는 수잔 민크위츠(Mrs Dr Susann Minkwitz)가 책임지고 있다. 현재 의장은 제레미 팅클러(Mr Jeremy Tinkler)이며 임기는 2026년 말까지다. ISO 기술 프로그램 관리자는 패트리샤 쿡(Mme Patricia Cook), ISO 편집 관리자는 산잘리 자인(Ms Sanjali Jain)등이다.범위는 해당 장치의 인간 임상 조사에 대한 우수 임상 실습 원칙 뿐 아니라 해당 재료 및 장치에 적용 가능한 생물학적 테스트 방법과 함께 의료 및 치과 재료 및 장치의 생물학적 및 임상 평가에 대한 접근 방식의 표준화다.현재 ISO/TC 194 사무국의 직접적인 책임 하에 발행된 표준은 37개 ISO/TC 194 사무국의 직접적인 책임 하에 개발 중인 표준은 16개다. 참여하고 있는 회원은 33개국, 참관 회원은 19개국이다.□ ISO/TC 194 사무국의 직접적인 책임 하에 발행된 표준 37개 중 15개 목록▷ISO 10993-1:2018 Biological evaluation of medical devices — Part 1: Evaluation and testing within a risk management process▷ISO 10993-2:2022 Biological evaluation of medical devices — Part 2: Animal welfare requirements▷ISO 10993-3:2014 Biological evaluation of medical devices — Part 3: Tests for genotoxicity, carcinogenicity and reproductive toxicity▷ISO 10993-4:2017 Biological evaluation of medical devices — Part 4: Selection of tests for interactions with blood▷ISO 10993-5:2009 Biological evaluation of medical devices — Part 5: Tests for in vitro cytotoxicity▷ISO 10993-6:2016 Biological evaluation of medical devices — Part 6: Tests for local effects after implantation▷ISO 10993-7:2008 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals▷ISO 10993-7:2008/Amd 1:2019 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals — Amendment 1: Applicability of allowable limits for neonates and infants▷ISO 10993-7:2008/Cor 1:2009 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals — Technical Corrigendum 1▷ISO 10993-9:2019 Biological evaluation of medical devices — Part 9: Framework for identification and quantification of potential degradation products▷ISO 10993-10:2021 Biological evaluation of medical devices — Part 10: Tests for skin sensitization▷ISO 10993-11:2017 Biological evaluation of medical devices — Part 11: Tests for systemic toxicity▷ISO 10993-12:2021 Biological evaluation of medical devices — Part 12: Sample preparation and reference materials▷ISO 10993-13:2010 Biological evaluation of medical devices — Part 13: Identification and quantification of degradation products from polymeric medical devices▷ISO 10993-14:2001 Biological evaluation of medical devices — Part 14: Identification and quantification of degradation products from ceramics□ ISO/TC 194 사무국의 직접적인 책임 하에 개발 중인 표준 16개 목록▷ISO/CD 8250 Cleanliness of medical devices — Process design and test methods▷ISO/CD 10993-1.2 Biological evaluation of medical devices — Part 1: Requirements and general principles for the evaluation of biological safety within a risk management process▷ISO/AWI 10993-2 Biological evaluation of medical devices — Part 2: Animal welfare requirements▷ISO/AWI 10993-3 Biological evaluation of medical devices — Part 3: Tests for genotoxicity, carcinogenicity and reproductive toxicity▷ISO 10993-4:2017/DAmd 1 Biological evaluation of medical devices — Part 4: Selection of tests for interactions with blood — Amendment 1▷ISO/CD 10993-6 Biological evaluation of medical devices — Part 6: Tests for local effects after implantation▷ISO/CD 10993-7.2 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals▷ISO/CD 10993-11 Biological evaluation of medical devices — Part 11: Tests for systemic toxicity▷ISO 10993-12:2021/AWI Amd 1 Biological evaluation of medical devices — Part 12: Sample preparation and reference materials — Amendment 1▷ISO/AWI 10993-16 Biological evaluation of medical devices — Part 16: Toxicokinetic study design for degradation products and leachables▷ISO 10993-17:2023/AWI Amd 1 Biological evaluation of medical devices — Part 17: Toxicological risk assessment of medical device constituents — Amendment 1▷ISO 10993-23:2021/AWI Amd 1 Biological evaluation of medical devices — Part 23: Tests for irritation — Amendment 1▷ISO/CD 14155 Clinical investigation of medical devices for human subjects — Good clinical practice▷ISO/AWI 18969 Clinical evaluation of medical devices▷ISO/AWI 21762 Medical devices utilizing human tissues and their derivatives — Application of risk management▷ISO/AWI TR 24850 Sources of hazard information for medical device constituents
[특집-기술위원회] TC 194 - 의료 장비의 생물학적 및 임상적 평가(Biological and clinical evaluation of medical devices)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~TC 67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~TC 107 △1963년 TC 108~TC 111 △1964년 TC 112~TC 115, TC 117 △1965년 TC 118 △1966년 TC 119~TC 122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146, TC 147, TC 148, TC 149, TC 150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~TC 161 △1975년 TC 162~TC 164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171, TC 172, TC 173, TC 174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~TC 186 △1984년 TC 188 △1985년 TC 189, TC 190, TC 191 등이 있다.ISO/TC 194 의료 장비의 생물학적 및 임상적 평가(Biological and clinical evaluation of medical devices)와 관련된 기술위원회는 TC 192, TC 193과 마찬가지로 1988년 결성됐다. 사무국은 독일 표준화기구(Deutsches Institut für Normung e.V., DIN)에서 맡고 있다.위원회는 수잔 민크위츠(Mrs Dr Susann Minkwitz)가 책임지고 있다. 현재 의장은 제레미 팅클러(Mr Jeremy Tinkler)이며 임기는 2026년 말까지다. ISO 기술 프로그램 관리자는 패트리샤 쿡(Mme Patricia Cook), ISO 편집 관리자는 산잘리 자인(Ms Sanjali Jain)등이다.범위는 해당 장치의 인간 임상 조사에 대한 우수 임상 실습 원칙 뿐 아니라 해당 재료 및 장치에 적용 가능한 생물학적 테스트 방법과 함께 의료 및 치과 재료 및 장치의 생물학적 및 임상 평가에 대한 접근 방식의 표준화다.현재 ISO/TC 194 사무국의 직접적인 책임 하에 발행된 표준은 37개 ISO/TC 194 사무국의 직접적인 책임 하에 개발 중인 표준은 16개다. 참여하고 있는 회원은 33개국, 참관 회원은 19개국이다.□ ISO/TC 194 사무국의 직접적인 책임 하에 발행된 표준 37개 중 15개 목록▷ISO 10993-1:2018 Biological evaluation of medical devices — Part 1: Evaluation and testing within a risk management process▷ISO 10993-2:2022 Biological evaluation of medical devices — Part 2: Animal welfare requirements▷ISO 10993-3:2014 Biological evaluation of medical devices — Part 3: Tests for genotoxicity, carcinogenicity and reproductive toxicity▷ISO 10993-4:2017 Biological evaluation of medical devices — Part 4: Selection of tests for interactions with blood▷ISO 10993-5:2009 Biological evaluation of medical devices — Part 5: Tests for in vitro cytotoxicity▷ISO 10993-6:2016 Biological evaluation of medical devices — Part 6: Tests for local effects after implantation▷ISO 10993-7:2008 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals▷ISO 10993-7:2008/Amd 1:2019 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals — Amendment 1: Applicability of allowable limits for neonates and infants▷ISO 10993-7:2008/Cor 1:2009 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals — Technical Corrigendum 1▷ISO 10993-9:2019 Biological evaluation of medical devices — Part 9: Framework for identification and quantification of potential degradation products▷ISO 10993-10:2021 Biological evaluation of medical devices — Part 10: Tests for skin sensitization▷ISO 10993-11:2017 Biological evaluation of medical devices — Part 11: Tests for systemic toxicity▷ISO 10993-12:2021 Biological evaluation of medical devices — Part 12: Sample preparation and reference materials▷ISO 10993-13:2010 Biological evaluation of medical devices — Part 13: Identification and quantification of degradation products from polymeric medical devices▷ISO 10993-14:2001 Biological evaluation of medical devices — Part 14: Identification and quantification of degradation products from ceramics□ ISO/TC 194 사무국의 직접적인 책임 하에 개발 중인 표준 16개 목록▷ISO/CD 8250 Cleanliness of medical devices — Process design and test methods▷ISO/CD 10993-1.2 Biological evaluation of medical devices — Part 1: Requirements and general principles for the evaluation of biological safety within a risk management process▷ISO/AWI 10993-2 Biological evaluation of medical devices — Part 2: Animal welfare requirements▷ISO/AWI 10993-3 Biological evaluation of medical devices — Part 3: Tests for genotoxicity, carcinogenicity and reproductive toxicity▷ISO 10993-4:2017/DAmd 1 Biological evaluation of medical devices — Part 4: Selection of tests for interactions with blood — Amendment 1▷ISO/CD 10993-6 Biological evaluation of medical devices — Part 6: Tests for local effects after implantation▷ISO/CD 10993-7.2 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals▷ISO/CD 10993-11 Biological evaluation of medical devices — Part 11: Tests for systemic toxicity▷ISO 10993-12:2021/AWI Amd 1 Biological evaluation of medical devices — Part 12: Sample preparation and reference materials — Amendment 1▷ISO/AWI 10993-16 Biological evaluation of medical devices — Part 16: Toxicokinetic study design for degradation products and leachables▷ISO 10993-17:2023/AWI Amd 1 Biological evaluation of medical devices — Part 17: Toxicological risk assessment of medical device constituents — Amendment 1▷ISO 10993-23:2021/AWI Amd 1 Biological evaluation of medical devices — Part 23: Tests for irritation — Amendment 1▷ISO/CD 14155 Clinical investigation of medical devices for human subjects — Good clinical practice▷ISO/AWI 18969 Clinical evaluation of medical devices▷ISO/AWI 21762 Medical devices utilizing human tissues and their derivatives — Application of risk management▷ISO/AWI TR 24850 Sources of hazard information for medical device constituents


![[특집-ISO/IEC JTC 1/SC 17 활동] 35. Result of voting on SR Ballot for ISO/](http://stdnews.kr/data/file/news/thumb/thumb-3555379571_4cufp2BH_756bcefa64e6169e58646ad7b061ecbec455fb11_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 34. Result of voting on SR ballot for ISO/](http://stdnews.kr/data/file/news/thumb/thumb-3555380113_kIQxAlfN_727cc6e35ccb9d5e6c07574a3b3a2ab9db104d48_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 33. Result of voting on SR ballot for ISO/](http://stdnews.kr/data/file/news/thumb/thumb-32068165_R52GPIij_2bca2660198a937d2534db7bfd9fc8174a76cfa2_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 32. Result of voting on SR Ballot for ISO/](http://stdnews.kr/data/file/news/thumb/thumb-32068165_TxRrtYEa_c36d1a53acc15db7e18fae132ffef64e11bda43c_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 31. Result of voting on SR Ballot for ISO/](http://stdnews.kr/data/file/news/thumb/thumb-3555377690_nrjmWhSf_d9b63299e7f3f52053141cae28f32f7df40b5918_340x240.jpg)


![[일본] 요코하마(横浜), 3월 원격근무로 일하는 50대 여성이 장시간 노동을 강요받아 적응장애가 발병해 산재로 인정받아](http://stdnews.kr/data/file/news/thumb/thumb-3555377672_BapV2SmF_41a011a26290be1daa3f6a5220df7b8b6d167f69_340x240.jpg)
![[인도] 마하라슈트라주 식품의약국(Maharashtra FDA), 맥도날드 상품명에 치즈를 잘못 표기해 소비자 기만 지적](http://stdnews.kr/data/file/news/thumb/thumb-3743818281_Uu5GpcKZ_6890f33f4b087f58686ed20e46a04bbb79ad883e_340x240.jpg)
![[남아공] 토코만 푸드(Thokoman Foods), 자사 땅콩버터 식품 안전성 재확인](http://stdnews.kr/data/file/news/thumb/thumb-3743818281_h5HrK0kT_c2453abdb4577a16b34590f5b8f76de9c2a95469_340x240.jpg)
![[일본] 혼다(ホンダ), 2030년까지 전기자동차(EV)를 중심으로 하는 전동화와 소트프웨어 개발에 10조 엔을 투자할 계획](http://stdnews.kr/data/file/news/thumb/thumb-3555381172_1g5z7YDN_4db7699b271b5e9dbbe1a4f6dc69fb01a9881abb_340x240.jpg)
![[일본] 자민당(自民党), 기업이 직원을 고객의 '카스하라(カスハラ)로부터 보호를 의무로 하는 방안을 고려 중](http://stdnews.kr/data/file/news/thumb/thumb-3555381172_PCNyaL1v_9f9b79d526b4be07024401e874fe26f618a42e7c_340x240.jpg)
![[일본] 총무성(総務省), 2023년 기준 전국의 빈집은 900만 호로 사상 최고치 기록](http://stdnews.kr/data/file/news/thumb/thumb-3555379571_qr01mWC9_fef7fa874e596585a04ee2dae235376595341779_340x240.jpg)
![[특집-기상기후재난] 한국중부발전(주) 신정철 선임 인터뷰 - 행정안전부 뿐 아니라 기상기후 연계조직 모두가 참여하는 협의체가](http://stdnews.kr/data/file/news/thumb/thumb-3555374516_iKWwUBas_9c1729f1e3977ee50c398986e7f98d5002a57deb_340x240.jpg)
![[특집-기상기후재난] (주)비밍코어 정성민 대표 인터뷰 - 인공지능(AI) 활용한 기후재난 대처 솔루션 개발](http://stdnews.kr/data/file/news/thumb/thumb-3555374391_0JZYhIcj_dca23c54fc7923952082a9d7af92db00b9dd33c9_340x240.jpg)
![[기획-표준 전문가] 한국투자증권 김범수 FC 인터뷰 - 표준전문가 양성 교육이 지속되길 희망](http://stdnews.kr/data/file/news/thumb/thumb-3555374114_Np9hM7aC_e6ffa916aade15e1c301badf3132ed3f0551a900_340x240.jpg)
![[특집-기상기후재난] 행정안전부 안전교육 전문인력 유정희 강사 인터뷰 - 기상기후재난예방 전문가 양성 시급](http://stdnews.kr/data/file/news/thumb/thumb-3555374240_gOmdLG10_cfc17ed887dccc93f503013bf794ed568a5d40dc_340x240.jpg)
![[특집-기상기후재난] (주)이토스 김형식 대표 인터뷰 - 재난을 사전에 예측·예방할 기술개발 시급](http://stdnews.kr/data/file/news/thumb/thumb-32068165_lmUrCBIn_797dc8926bb7d90542546463cc73e6233f0bbb46_340x240.png)