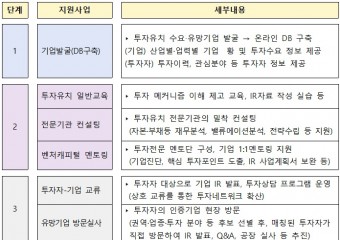
검색결과
-
![[스위스] 세계보건기구(WHO), 국제전기통신연합(ITU)과 공동으로 원격의료 서비스 접근성에 관한 표준 개발](http://stdnews.kr/data/file/news/thumb/thumb-988342002_bBZoRL6w_9c73fbd228fbdb066e9749a43e4872152d6733e6_200x180.jpg) [스위스] 세계보건기구(WHO), 국제전기통신연합(ITU)과 공동으로 원격의료 서비스 접근성에 관한 표준 개발세계보건기구(World Health Organization, WHO)에 따르면 국제전기통신연합(International Telecommunication Union, ITU)과 공동으로 원격의료 서비스(telehealth services)의 접근성에 대한 글로벌 표준을 개발했다.개발된 표준은 원격 의료 플랫폼이 접근 가능한 원격 의료 서비스 제공을 보장하기 위해 반드시 갖춰야 될 기술적 요구사항 목록을 제공하고 있다.모든 요구사항은 시민사회와 산업계로부터 수집된 종합적인 피드백 및 의견뿐 아니라 최고로 이용 가능한 근거에 기반을 두고 있다.표준 요건은 규정이나 법률로서 회원국들에 의해 채택되도록 한 것이다. 의료 전문가나 제조업체가 자발적으로 이행해야 된다.원격의료 서비스의 접근성을 위한 WHO-ITU 세계 표준은 2022년 6월 16일 장애인권리협약 당사국총회(Conference of State Parties to the Convention on the Rights of Persons with Disabilities) 제15차 회기 중 공식 출범했다.코로나19(COVID-19) 팬데믹 기간 많은 국가에서 원격 의료 서비스 활용이 크게 증가했으며 일반인들의 기본 요구사항이 됐다. 반면 많은 장애인들은 원격 의료 서비스에 접속하고 사용하는데 어려움을 겪었다.예를 들어 원격의료 플랫폼은 시각 장애가 있는 사람들이 정보에 접근할 수 있는 화면 판독기와 같은 장치와의 호환문제가 발생됐다.또한 화상회의에서 자막이나 볼륨 조절 불량으로 청각 장애가 있거나 청각 장애인 들이 의료 전문가와 원격상호 작용에 실패하는 경우가 발생했다.따라서 세계보건기구(WHO)와 국제전기통신연합(ITU)은 공동으로 글로벌 표준 개발을 통해 장애인들의 원격의료 서비스 접근성을 높이기 위해 노력하고 있다.
[스위스] 세계보건기구(WHO), 국제전기통신연합(ITU)과 공동으로 원격의료 서비스 접근성에 관한 표준 개발세계보건기구(World Health Organization, WHO)에 따르면 국제전기통신연합(International Telecommunication Union, ITU)과 공동으로 원격의료 서비스(telehealth services)의 접근성에 대한 글로벌 표준을 개발했다.개발된 표준은 원격 의료 플랫폼이 접근 가능한 원격 의료 서비스 제공을 보장하기 위해 반드시 갖춰야 될 기술적 요구사항 목록을 제공하고 있다.모든 요구사항은 시민사회와 산업계로부터 수집된 종합적인 피드백 및 의견뿐 아니라 최고로 이용 가능한 근거에 기반을 두고 있다.표준 요건은 규정이나 법률로서 회원국들에 의해 채택되도록 한 것이다. 의료 전문가나 제조업체가 자발적으로 이행해야 된다.원격의료 서비스의 접근성을 위한 WHO-ITU 세계 표준은 2022년 6월 16일 장애인권리협약 당사국총회(Conference of State Parties to the Convention on the Rights of Persons with Disabilities) 제15차 회기 중 공식 출범했다.코로나19(COVID-19) 팬데믹 기간 많은 국가에서 원격 의료 서비스 활용이 크게 증가했으며 일반인들의 기본 요구사항이 됐다. 반면 많은 장애인들은 원격 의료 서비스에 접속하고 사용하는데 어려움을 겪었다.예를 들어 원격의료 플랫폼은 시각 장애가 있는 사람들이 정보에 접근할 수 있는 화면 판독기와 같은 장치와의 호환문제가 발생됐다.또한 화상회의에서 자막이나 볼륨 조절 불량으로 청각 장애가 있거나 청각 장애인 들이 의료 전문가와 원격상호 작용에 실패하는 경우가 발생했다.따라서 세계보건기구(WHO)와 국제전기통신연합(ITU)은 공동으로 글로벌 표준 개발을 통해 장애인들의 원격의료 서비스 접근성을 높이기 위해 노력하고 있다. -
![[미국] 노동부, 공정근로기준법(LSA) 하에서 고용인 대 독립 계약자 분석에 관한 새로운 최종 규칙 개발 계획](http://stdnews.kr/img/no_image_282_80.png) [미국] 노동부, 공정근로기준법(LSA) 하에서 고용인 대 독립 계약자 분석에 관한 새로운 최종 규칙 개발 계획미국 노동부(U.S. Department of Labor, DOL)에 따르면 2022년 6월 공정근로기준법(Fair Labor Standards Act, FLSA) 하에서 고용인 대 독립 계약자 분석에 관한 새로운 최종 규칙을 개발할 계획이다.현재 독립 계약자(IC) 최종 규칙은 이전 트럼프 행정부에서 제정됐다. 트럼프 행정부가 제정한 규칙은 2021년 3월까지만 유효했지만 2021년 5월 노동부는 조치를 연기했다.2022년 3월 텍사스주 연방법원은 노동부가 해당 규칙을 연기 및 철회한 것은 불법이라고 판단했다. 또한 현행 최종 규칙은 2021년 3월 이후 여전히 유효하다고 인정했다.따라서 노동부는 해당 판결에 대해 항소했으며, 소송은 미국 연방고등법원에 계류돼 있다. 지난 몇년 동안 법원과 노동부는 개인이 고용인 혹은 독립 계약자인지에 관해 비슷하지만 조금 차이가 있는 기준을 적용했다.판단의 기준은 고용주와 개인 사이 관계의 '경제적 실재(economic reality)'에 초점을 맞춘다. 대법원은 United States v. Silk와 331 U.S. 704 (1947), and Rutherford Food Corp. v. McComb, 331 U.S. 722(1947) 2개 사건을 판단하면서 6개의 고려사항을 제시했다.세부 내역을 살펴보면 △작업에 대한 고용주와 개인의 통제 정도 △이익과 손실에 대한 개인의 기회 △설비와 장비에 대한 개인의 투자 △양자 사이의 관계 영속성 △개인에게 요구되는 기술 혹은 전문성 △작업이 생산의 통합 단위 부문인지 여부 등이다.개별 요소에 가중치를 주지 않거나 평균 가중치를 적용하는 대신에 독립계약자(IC) 최종 규칙은 작업에 대한 개인 통제의 본질과 정도, 이익 혹은 손실에 대한 개인의 기회 2가지 핵심 요소를 비교 분석한다.독립계약자(IC) 최종 규칙은 2가지 요소가 가장 증명력이 높으므로 가장 큰 가중치를 부여해야 한다고 주장한다. 하지만 이들 2가지 요소만으로 결론을 내리지 않고, 개인에게 요구되는 기술 혹은 전문성, 양자 사이 관계의 영속성, 작업이 생산의 통합 단위 부문인지 여부 등 3가지 요인도 고려돼야 한다.현재 노동부는 노동자가 고용인인지 혹은 독립 계약자인지에 따라 공정근로기준법(FLSA)에 따라 보호돼야 한다고 판단하고 있다. 긱 경제(Gig economy)에서 독립 계약자가 급증하면서 경제의 핵심축으로 부상했기 때문이다.연방정부가 연방법에 따라 최종 규칙을 정한다고 하더라도 캘리포니아주와 같은 일부 주에서는 자체 법률에 따라 독립 계약자인지 판단한다.더불어 현재 독립 계약자(IC) 최종 규칙은 내국세입법(Internal Revenue Code), 전국노동관계법(National Labor Relations Act) 혹은 기타 연방법률 하에서 규정한 독립계약자를 다시 정의하지는 않는다.
[미국] 노동부, 공정근로기준법(LSA) 하에서 고용인 대 독립 계약자 분석에 관한 새로운 최종 규칙 개발 계획미국 노동부(U.S. Department of Labor, DOL)에 따르면 2022년 6월 공정근로기준법(Fair Labor Standards Act, FLSA) 하에서 고용인 대 독립 계약자 분석에 관한 새로운 최종 규칙을 개발할 계획이다.현재 독립 계약자(IC) 최종 규칙은 이전 트럼프 행정부에서 제정됐다. 트럼프 행정부가 제정한 규칙은 2021년 3월까지만 유효했지만 2021년 5월 노동부는 조치를 연기했다.2022년 3월 텍사스주 연방법원은 노동부가 해당 규칙을 연기 및 철회한 것은 불법이라고 판단했다. 또한 현행 최종 규칙은 2021년 3월 이후 여전히 유효하다고 인정했다.따라서 노동부는 해당 판결에 대해 항소했으며, 소송은 미국 연방고등법원에 계류돼 있다. 지난 몇년 동안 법원과 노동부는 개인이 고용인 혹은 독립 계약자인지에 관해 비슷하지만 조금 차이가 있는 기준을 적용했다.판단의 기준은 고용주와 개인 사이 관계의 '경제적 실재(economic reality)'에 초점을 맞춘다. 대법원은 United States v. Silk와 331 U.S. 704 (1947), and Rutherford Food Corp. v. McComb, 331 U.S. 722(1947) 2개 사건을 판단하면서 6개의 고려사항을 제시했다.세부 내역을 살펴보면 △작업에 대한 고용주와 개인의 통제 정도 △이익과 손실에 대한 개인의 기회 △설비와 장비에 대한 개인의 투자 △양자 사이의 관계 영속성 △개인에게 요구되는 기술 혹은 전문성 △작업이 생산의 통합 단위 부문인지 여부 등이다.개별 요소에 가중치를 주지 않거나 평균 가중치를 적용하는 대신에 독립계약자(IC) 최종 규칙은 작업에 대한 개인 통제의 본질과 정도, 이익 혹은 손실에 대한 개인의 기회 2가지 핵심 요소를 비교 분석한다.독립계약자(IC) 최종 규칙은 2가지 요소가 가장 증명력이 높으므로 가장 큰 가중치를 부여해야 한다고 주장한다. 하지만 이들 2가지 요소만으로 결론을 내리지 않고, 개인에게 요구되는 기술 혹은 전문성, 양자 사이 관계의 영속성, 작업이 생산의 통합 단위 부문인지 여부 등 3가지 요인도 고려돼야 한다.현재 노동부는 노동자가 고용인인지 혹은 독립 계약자인지에 따라 공정근로기준법(FLSA)에 따라 보호돼야 한다고 판단하고 있다. 긱 경제(Gig economy)에서 독립 계약자가 급증하면서 경제의 핵심축으로 부상했기 때문이다.연방정부가 연방법에 따라 최종 규칙을 정한다고 하더라도 캘리포니아주와 같은 일부 주에서는 자체 법률에 따라 독립 계약자인지 판단한다.더불어 현재 독립 계약자(IC) 최종 규칙은 내국세입법(Internal Revenue Code), 전국노동관계법(National Labor Relations Act) 혹은 기타 연방법률 하에서 규정한 독립계약자를 다시 정의하지는 않는다. -
![[멕시코] 대법원(Supreme Court of Mexico), 저작권 위반으로부터 초래된 피해의 정량화에 대한 기준 공개](http://stdnews.kr/data/file/news/thumb/thumb-988342002_bNnH1QZC_a2790355670aa271017daca4a50319dca63233c6_200x180.jpg) [멕시코] 대법원(Supreme Court of Mexico), 저작권 위반으로부터 초래된 피해의 정량화에 대한 기준 공개멕시코 대법원(Supreme Court of Mexico)에 따르면 2022년 6월 저작권 위반으로부터 초래된 피해의 정량화에 대한 기준을 공개했다.해당 기준은 저작권법 위반으로 인해 초래된 피해를 산정한 연방저작권법 제216조에 기반했다. 제216조는 원 제품의 판매와 서비스의 연주(연기) 가격의 최소 40% 이상으로 정했다.나이트클럽을 운영하며 저작권법 위반으로 기소된 기업은 해당 조항이 위헌이라고 주장했다. 저작권법이 법률 명확성과 비례성 즉 과잉금지의 원칙을 위배했다는 것이다.저작권법에서 보상의 비율에 적용되는 수입을 규정하는 것은 불가능하기 때문이다. 해당 기업은 나이트클럽에서 음악을 연주하며 저작권법을 위반했다.하지만 나이트클럽의 수입은 음악의 연주와 더불어 음료와 음식 서비스가 제공하므로 수입에서 식음료 서비스 요금은 제외해야 한다는 입장이다.또한 식자재의 구입비, 관리비, 세금 등도 수입에 포함해서는 안된다는 주장이다. 어떤 경우라도 피해 보상은 나이트클럽에 의해 창출된 수입으로 한정돼야 한다는 것이다.대법원은 저작권법 제 216조는 해당 조항이 피해 보상금을 계산하기 위해 2가지 시스템을 제공하 때문에 합헌이라고 간주했다.2가지 시스템은 다음과 같다. 하나는 보상금은 원 제품의 판매와 서비스의 연주(연기) 가격의 최소 40%로 정해야 한다는 것이다. 다른 하나는 보상금을 계산하기 어렵다면 전문가의 지원으로 결정해야 한다는 조건이다.보상금은 처벌의 목적이 아니라 저작권을 위반해 초래된 피해를 보상하기 위한 것이라고 판단했다. 또한 서비스의 연주(연기)의 위반 사건에서 보상금은 저작권법의 위반과 관련된 총수입을 포함해 계산해야 한다.나이트클럽의 사건에서 대법원은 음식과 음료수의 판매도 보상금 산정에 포함해야 한다고 판단했다. 음악의 연주가 음식과 음료수의 판매에 기여하기 때문이다.
[멕시코] 대법원(Supreme Court of Mexico), 저작권 위반으로부터 초래된 피해의 정량화에 대한 기준 공개멕시코 대법원(Supreme Court of Mexico)에 따르면 2022년 6월 저작권 위반으로부터 초래된 피해의 정량화에 대한 기준을 공개했다.해당 기준은 저작권법 위반으로 인해 초래된 피해를 산정한 연방저작권법 제216조에 기반했다. 제216조는 원 제품의 판매와 서비스의 연주(연기) 가격의 최소 40% 이상으로 정했다.나이트클럽을 운영하며 저작권법 위반으로 기소된 기업은 해당 조항이 위헌이라고 주장했다. 저작권법이 법률 명확성과 비례성 즉 과잉금지의 원칙을 위배했다는 것이다.저작권법에서 보상의 비율에 적용되는 수입을 규정하는 것은 불가능하기 때문이다. 해당 기업은 나이트클럽에서 음악을 연주하며 저작권법을 위반했다.하지만 나이트클럽의 수입은 음악의 연주와 더불어 음료와 음식 서비스가 제공하므로 수입에서 식음료 서비스 요금은 제외해야 한다는 입장이다.또한 식자재의 구입비, 관리비, 세금 등도 수입에 포함해서는 안된다는 주장이다. 어떤 경우라도 피해 보상은 나이트클럽에 의해 창출된 수입으로 한정돼야 한다는 것이다.대법원은 저작권법 제 216조는 해당 조항이 피해 보상금을 계산하기 위해 2가지 시스템을 제공하 때문에 합헌이라고 간주했다.2가지 시스템은 다음과 같다. 하나는 보상금은 원 제품의 판매와 서비스의 연주(연기) 가격의 최소 40%로 정해야 한다는 것이다. 다른 하나는 보상금을 계산하기 어렵다면 전문가의 지원으로 결정해야 한다는 조건이다.보상금은 처벌의 목적이 아니라 저작권을 위반해 초래된 피해를 보상하기 위한 것이라고 판단했다. 또한 서비스의 연주(연기)의 위반 사건에서 보상금은 저작권법의 위반과 관련된 총수입을 포함해 계산해야 한다.나이트클럽의 사건에서 대법원은 음식과 음료수의 판매도 보상금 산정에 포함해야 한다고 판단했다. 음악의 연주가 음식과 음료수의 판매에 기여하기 때문이다. -
![[프랑스] 바이오콥(BIOCORP), 맬리아(Mallya) 장비 FDA 510(k) 승인 획득](http://stdnews.kr/data/file/news/thumb/thumb-2944253047_HyZPbxON_479f4166a8e5d428acc46a487347c2bde8ab9161_200x180.jpg) [프랑스] 바이오콥(BIOCORP), 맬리아(Mallya) 장비 FDA 510(k) 승인 획득프랑스 의료기기 설계, 개발, 제조 전문 기업 바이오콥(BIOCORP)에 따르면 최근 미국 식품의약국(U.S. Food & Drug Administration, FDA)으로부터 510(K) 승인을 받았다.승인은 인슐린 펜을 연결하는 스마트 의료기기인 맬리아(Mallya)가 대상이다. 이 규제 프로세스에 깊이 관여한 모든 직원 및 바이오콥의 중요한 성과로 자리매김됐다.특히 FDA 승인은 바이오콥이 가장 높은 규제 요구사항을 충족할 수 있는 능력을 갖췄다는 것을 입증한다. 미국 시장에서 맬리아 장치를 상업적으로 출시할 수 있는 발판이 될 것으로 전망된다. 맬리아의 FDA승인 소식은 모든 업계 파트너들이 세계 최대 당뇨병 시장에서 맬리아를 상업화하기 위해 간절히 기다려온 소식이다. 아울러 미국 환자들도 맬리아의 서비스 혜택을 누릴 수 있게 됐다.승인을 받음에 따라 2023년 바이오콥의 판매에 긍정적인 영향을 획득할 수 있을 뿐만 아니라 스마트 펜 분야 리더로 성장할 것으로 전망된다.맬리아 의료기기는 인슐린 펜 주사기에 직접 부착돼 장치를 연결하는 스마트 센서다. 선택한 인슐린 단위, 주입 날짜 및 시간 등 주요 치료 정보를 자동으로 수집 및 기록하고 전용 디지털 애플리케이션으로 전송한다.맬리아는 SANOFI의 Solostar 펜 주사기와 호환되는 초기 버전과 함께 다양한 유형의 인슐린 및 GLP-1 약물을 자동으로 연결할 수 있는 시스템이다. 미국에서 최로 승인을 받았다.맬리아는 Class IIb 의료기기로 CE 마크를 받았다. Class IIb는 해당 치료나 술기(시술, 기구, 기기의 준말)의 효과가 잘 정립되지 않았으나 시행해 볼 수 있는 정도를 의미한다.
[프랑스] 바이오콥(BIOCORP), 맬리아(Mallya) 장비 FDA 510(k) 승인 획득프랑스 의료기기 설계, 개발, 제조 전문 기업 바이오콥(BIOCORP)에 따르면 최근 미국 식품의약국(U.S. Food & Drug Administration, FDA)으로부터 510(K) 승인을 받았다.승인은 인슐린 펜을 연결하는 스마트 의료기기인 맬리아(Mallya)가 대상이다. 이 규제 프로세스에 깊이 관여한 모든 직원 및 바이오콥의 중요한 성과로 자리매김됐다.특히 FDA 승인은 바이오콥이 가장 높은 규제 요구사항을 충족할 수 있는 능력을 갖췄다는 것을 입증한다. 미국 시장에서 맬리아 장치를 상업적으로 출시할 수 있는 발판이 될 것으로 전망된다. 맬리아의 FDA승인 소식은 모든 업계 파트너들이 세계 최대 당뇨병 시장에서 맬리아를 상업화하기 위해 간절히 기다려온 소식이다. 아울러 미국 환자들도 맬리아의 서비스 혜택을 누릴 수 있게 됐다.승인을 받음에 따라 2023년 바이오콥의 판매에 긍정적인 영향을 획득할 수 있을 뿐만 아니라 스마트 펜 분야 리더로 성장할 것으로 전망된다.맬리아 의료기기는 인슐린 펜 주사기에 직접 부착돼 장치를 연결하는 스마트 센서다. 선택한 인슐린 단위, 주입 날짜 및 시간 등 주요 치료 정보를 자동으로 수집 및 기록하고 전용 디지털 애플리케이션으로 전송한다.맬리아는 SANOFI의 Solostar 펜 주사기와 호환되는 초기 버전과 함께 다양한 유형의 인슐린 및 GLP-1 약물을 자동으로 연결할 수 있는 시스템이다. 미국에서 최로 승인을 받았다.맬리아는 Class IIb 의료기기로 CE 마크를 받았다. Class IIb는 해당 치료나 술기(시술, 기구, 기기의 준말)의 효과가 잘 정립되지 않았으나 시행해 볼 수 있는 정도를 의미한다. -
![[미국] 퀄리트루(QualiTru), 5월 ISO 9001:2015 인증 획득](http://stdnews.kr/data/file/news/thumb/thumb-988342002_lbnjduMA_9d4429662ef29c0d36d3932f1c3179cf5a27664e_200x180.jpg) [미국] 퀄리트루(QualiTru), 5월 ISO 9001:2015 인증 획득미국 유동식 샘플링 시장업체인 퀄리트루 샘플링 시스템(QualiTru Sampling Systems)에 따르면 2022년 5월 ISO 9001:2015 인증을 획득했다. 이전 기업의 명칭은 QMI이었다.유동식(liquid food)은 고형성분이 없으므로 씹지 않고 그대로 삼킬 수 있는 음식물을 말한다. 열량과 영양소의 보급은 충분하지 않고 수분을 섭취하기 위한 목적으로 먹는다.ISO 9001:2015 표준은 유동식 산업을 위한 무균 샘플링 제품, 시스템, 서비스에 관련됐다. 따라서 인증을 받았다는 것은 무균을 위한 제품의 품질을 최고 수준으로 제공함을 의미한다. 이전에는 자사의 TruStream Stainless Steel Ports와 TruStream Septa가 3-A 위생 표준 인증을 받았다. 표준 63-04를 충족한다. 해당 표준은 처리 장비와 시스템에서 고결성과 위생을 위한 최고 산업 표준 레벨이다.퀼리트루의 기술력은 미국 식품의약국(FDA)의 A등급의 6장을 인용했다. 멸균우유규정은(Pasteurized Milk Ordinance, PMO)은 농장의 대용량 우유 탱크나 사일로부터 처리를 위해 운송된 우유에까지 직접 샘플을 수집하도록 요구한다.지난 40여년 동안 멸균 액체 샘플링 과학에서 선두주자로 자리매김해왔다. 자체 개발한 혁신적이고 편리하며 다용도이면서 비용 효과적인 샘플링 시스템은 전 세게적으로 통용된다.특히 전체 공급망을 통해 유제품이나 유동식 품질을 검증하기 위해 미생물학적인 테스트도 진행한다. 대용량 탱크나 사일로에서 멸균 생픔 테스트와 품질 확인은 중요한 과정에 속한다.참고로 퀼리트루는 1983년 설립됐으며 다른 기업이 제공하기 어려운 독특한 멸균과 대표 샘플링의 조합을 제공한다. 고객과 파트너를 위해 문제 해결 접근법을 선택한다.
[미국] 퀄리트루(QualiTru), 5월 ISO 9001:2015 인증 획득미국 유동식 샘플링 시장업체인 퀄리트루 샘플링 시스템(QualiTru Sampling Systems)에 따르면 2022년 5월 ISO 9001:2015 인증을 획득했다. 이전 기업의 명칭은 QMI이었다.유동식(liquid food)은 고형성분이 없으므로 씹지 않고 그대로 삼킬 수 있는 음식물을 말한다. 열량과 영양소의 보급은 충분하지 않고 수분을 섭취하기 위한 목적으로 먹는다.ISO 9001:2015 표준은 유동식 산업을 위한 무균 샘플링 제품, 시스템, 서비스에 관련됐다. 따라서 인증을 받았다는 것은 무균을 위한 제품의 품질을 최고 수준으로 제공함을 의미한다. 이전에는 자사의 TruStream Stainless Steel Ports와 TruStream Septa가 3-A 위생 표준 인증을 받았다. 표준 63-04를 충족한다. 해당 표준은 처리 장비와 시스템에서 고결성과 위생을 위한 최고 산업 표준 레벨이다.퀼리트루의 기술력은 미국 식품의약국(FDA)의 A등급의 6장을 인용했다. 멸균우유규정은(Pasteurized Milk Ordinance, PMO)은 농장의 대용량 우유 탱크나 사일로부터 처리를 위해 운송된 우유에까지 직접 샘플을 수집하도록 요구한다.지난 40여년 동안 멸균 액체 샘플링 과학에서 선두주자로 자리매김해왔다. 자체 개발한 혁신적이고 편리하며 다용도이면서 비용 효과적인 샘플링 시스템은 전 세게적으로 통용된다.특히 전체 공급망을 통해 유제품이나 유동식 품질을 검증하기 위해 미생물학적인 테스트도 진행한다. 대용량 탱크나 사일로에서 멸균 생픔 테스트와 품질 확인은 중요한 과정에 속한다.참고로 퀼리트루는 1983년 설립됐으며 다른 기업이 제공하기 어려운 독특한 멸균과 대표 샘플링의 조합을 제공한다. 고객과 파트너를 위해 문제 해결 접근법을 선택한다. -
![[미국] 의료기기 재처리자 협회(AMDR), 일회용 의료기기 재처리 및 재제조에 대한 글로벌 규제 표준 발표](http://stdnews.kr/data/file/news/thumb/thumb-988342002_xdlEBUQy_298f72a4629cc0ff7287a41e62c1f891d98efd58_200x180.jpg) [미국] 의료기기 재처리자 협회(AMDR), 일회용 의료기기 재처리 및 재제조에 대한 글로벌 규제 표준 발표미국 의료기기 재처리자 협회(Association of Medical Device Reprocessors, AMDR)에 따르면 일회용 의료기기 재처리 및 재제조에 대한 최초 글로벌 규제 표준을 발표했다.글로벌 규제 표준 보고서는 전 세계적으로 재처리(유럽에서는 재제조라고 함) 관행을 관리하는 모든 알려진 규정, 표준, 지침 등이 포함돼 있다.또한 더 많은 국가의 규제 당국이 더 많은 병원이 폐기물을 줄일 수 있는 합법적이고 안전하며 효과적인 프로세스를 만들 수 있도록 로드맵을 제공하고 있다.전 세계 병원과 의료 시스템에 이러한 혜택을 제공하기 위해 인증기관, 보건부, 의료기기 규제 당국이 지원하는 첫 번째 로드맵이다.의료 시스템과 병원이 규정에 맞는 재처리된 일회용 기기를 사용할 경우 환자의 안전을 해치지 않고 시술비를 절감할 수 있다.재처리된 일회용 기기 사용으로 공급망 탄력성을 구축하고 정부와 병원이 탄소 배출량을 더 빨리 제로로 만들 수 있도록 지원할 수 있다.일회용 의료기기를 재처리 하는 병원은 온실가스 배출량, 비용, 낭비 등을 줄일 수 있다. 따라서 연간 수억 달러를 절약할 수 있을 것으로 추정된다.미국 식품의약국(Food and Drug Administration, FDA)은 세계 최초로 상업적 SUD 재처리를 위한 길을 만든 규제 당국이다.현재 3100만 개 이상의 SUD가 재처리 되고 있으며 환자 안전에 대한 위험 증가 없이 안전하게 재사용 되고 있다. FDA는 이 장치를 원래 장치와 실질적으로 동등한 것으로 간주하고 있다.
[미국] 의료기기 재처리자 협회(AMDR), 일회용 의료기기 재처리 및 재제조에 대한 글로벌 규제 표준 발표미국 의료기기 재처리자 협회(Association of Medical Device Reprocessors, AMDR)에 따르면 일회용 의료기기 재처리 및 재제조에 대한 최초 글로벌 규제 표준을 발표했다.글로벌 규제 표준 보고서는 전 세계적으로 재처리(유럽에서는 재제조라고 함) 관행을 관리하는 모든 알려진 규정, 표준, 지침 등이 포함돼 있다.또한 더 많은 국가의 규제 당국이 더 많은 병원이 폐기물을 줄일 수 있는 합법적이고 안전하며 효과적인 프로세스를 만들 수 있도록 로드맵을 제공하고 있다.전 세계 병원과 의료 시스템에 이러한 혜택을 제공하기 위해 인증기관, 보건부, 의료기기 규제 당국이 지원하는 첫 번째 로드맵이다.의료 시스템과 병원이 규정에 맞는 재처리된 일회용 기기를 사용할 경우 환자의 안전을 해치지 않고 시술비를 절감할 수 있다.재처리된 일회용 기기 사용으로 공급망 탄력성을 구축하고 정부와 병원이 탄소 배출량을 더 빨리 제로로 만들 수 있도록 지원할 수 있다.일회용 의료기기를 재처리 하는 병원은 온실가스 배출량, 비용, 낭비 등을 줄일 수 있다. 따라서 연간 수억 달러를 절약할 수 있을 것으로 추정된다.미국 식품의약국(Food and Drug Administration, FDA)은 세계 최초로 상업적 SUD 재처리를 위한 길을 만든 규제 당국이다.현재 3100만 개 이상의 SUD가 재처리 되고 있으며 환자 안전에 대한 위험 증가 없이 안전하게 재사용 되고 있다. FDA는 이 장치를 원래 장치와 실질적으로 동등한 것으로 간주하고 있다. -
![[미국] 국제전기기술위원회(IEC)와 국제표준기구(ISO), 최근 사이버보안 표준 IEC 81001-5-1:2021 발표](http://stdnews.kr/data/file/news/thumb/thumb-988342002_NZAjVCTi_dc96781cbb3091562fc9a0322a58d8a65bbe5ceb_200x180.jpg) [미국] 국제전기기술위원회(IEC)와 국제표준기구(ISO), 최근 사이버보안 표준 IEC 81001-5-1:2021 발표국제전기기술위원회(International Electrotechnical Commission, IEC)와 국제표준기구(International Organization for Standards, ISO)에 따르면 최근 사이버보안 표준을 발표했다.새로운 표준은 건강 소프트웨어 및 건강 IT 사이버보안을 위한 의료 기기 소프트웨어 개발 표준에 관한 것이다. 기기 및 비기기 건강 소프트웨어 관련 기업의 사업에 상당한 영형을 미칠 수 있다.발표된 표준은 IEC 81001-5-1:2021로 일련의 IEC 81001 건강 소프트웨어 표준이 될 것으로 예상된다. 표준의 범위는 건강 관련 사용을 위해 특별히 고안된 하드웨어의 일부인 소프트웨어, 의료 기기로서의 소프트웨어, 기타 건강 관련 용도를 위한 소프트웨어 전용 제품 등 의료 기기 소프트웨어이다.새로운 표준의 가장 중요한 특징은 IEC 62304:2006과 AMD1:2015(Medical device software – software life cycle processes) 표준을 활동 및 결과물의 기초로 사용하고 각 IEC 62304 프로세스 단계에 사이버보안 요구사항을 포함한 것이다.의료기기 제조사들 사이에는 흔한 일이지만 IEC 62304 표준은 회사가 이전에 고려하지 않았을 수 있는 비기기 건강 소프트웨어 회사에 일련의 수명주기활동을 부과할 수 있다.IEC 81001-5-1:2021의 부록 A에 IEC 62304을 따르는 것이 IEC 81001-5-1:2021을 준수하기 위한 요구사항이 아니라고 명시돼 있다.하지만 IEC 81001-5-1의 준수시 IEC 62304 표준과 일치하지 않을 경우 출처를 알 수 없는 소프트웨어, 소프트웨어 아키텍처 설계, 안전 위험 관리, 문제해결, 요구사항 및 아키텍처, 설계에 대한 문서화된 고정된 검토에 관한 요구 사항 등에서 문제의 소지가 있을 수 있다.새로운 표준은 안전위험 관리와 상관관계가 있지만 안전에 영향을 미치는 것 이상의 사이버 보안 취약성과 위협 등 새로운 위험을 고려하고 있다.이 표준은 미국 AAMI(Association for the Advancement of Medical Instrumentation), NIST(National Institute for Standards and Technology), 유럽 MDGC(Medical Device Consortium Group) 등 다양한 출처의 사이버보안 지침과 일치하고 있다.다만 사이버보안 위험을 안전관련 문제로 제한하는 미국 FDA(Food and Drug Administration)의 사이버보안 지침과는 일치하지 않는다. 자세한 내용은 IEC 81001-5-1:2021 표준에서 확인이 가능하다.
[미국] 국제전기기술위원회(IEC)와 국제표준기구(ISO), 최근 사이버보안 표준 IEC 81001-5-1:2021 발표국제전기기술위원회(International Electrotechnical Commission, IEC)와 국제표준기구(International Organization for Standards, ISO)에 따르면 최근 사이버보안 표준을 발표했다.새로운 표준은 건강 소프트웨어 및 건강 IT 사이버보안을 위한 의료 기기 소프트웨어 개발 표준에 관한 것이다. 기기 및 비기기 건강 소프트웨어 관련 기업의 사업에 상당한 영형을 미칠 수 있다.발표된 표준은 IEC 81001-5-1:2021로 일련의 IEC 81001 건강 소프트웨어 표준이 될 것으로 예상된다. 표준의 범위는 건강 관련 사용을 위해 특별히 고안된 하드웨어의 일부인 소프트웨어, 의료 기기로서의 소프트웨어, 기타 건강 관련 용도를 위한 소프트웨어 전용 제품 등 의료 기기 소프트웨어이다.새로운 표준의 가장 중요한 특징은 IEC 62304:2006과 AMD1:2015(Medical device software – software life cycle processes) 표준을 활동 및 결과물의 기초로 사용하고 각 IEC 62304 프로세스 단계에 사이버보안 요구사항을 포함한 것이다.의료기기 제조사들 사이에는 흔한 일이지만 IEC 62304 표준은 회사가 이전에 고려하지 않았을 수 있는 비기기 건강 소프트웨어 회사에 일련의 수명주기활동을 부과할 수 있다.IEC 81001-5-1:2021의 부록 A에 IEC 62304을 따르는 것이 IEC 81001-5-1:2021을 준수하기 위한 요구사항이 아니라고 명시돼 있다.하지만 IEC 81001-5-1의 준수시 IEC 62304 표준과 일치하지 않을 경우 출처를 알 수 없는 소프트웨어, 소프트웨어 아키텍처 설계, 안전 위험 관리, 문제해결, 요구사항 및 아키텍처, 설계에 대한 문서화된 고정된 검토에 관한 요구 사항 등에서 문제의 소지가 있을 수 있다.새로운 표준은 안전위험 관리와 상관관계가 있지만 안전에 영향을 미치는 것 이상의 사이버 보안 취약성과 위협 등 새로운 위험을 고려하고 있다.이 표준은 미국 AAMI(Association for the Advancement of Medical Instrumentation), NIST(National Institute for Standards and Technology), 유럽 MDGC(Medical Device Consortium Group) 등 다양한 출처의 사이버보안 지침과 일치하고 있다.다만 사이버보안 위험을 안전관련 문제로 제한하는 미국 FDA(Food and Drug Administration)의 사이버보안 지침과는 일치하지 않는다. 자세한 내용은 IEC 81001-5-1:2021 표준에서 확인이 가능하다. -
![[인도] 뉴레카, 분무기 및 혈압 모니터에 국제표준 ISO 13485:2016 인증 획득](http://stdnews.kr/data/file/news/thumb/thumb-2949739381_uYq8RxL9_09adf0d85d7dadf51e5dd62b85887f0f13ca2a29_200x180.jpg) [인도] 뉴레카, 분무기 및 혈압 모니터에 국제표준 ISO 13485:2016 인증 획득인도 헬스케어 기업인 뉴레카(Nureca)에 따르면 분무기 및 혈압 모니터에 대해 국제표준 ISO 13485:2016 인증을 획득했다. ISO 13485:2016 표준은 의료기기 품질경영시스템과 관련돼 있다.인증은 뉴레카가 전액 출자한 자회사인 뉴레카테크놀로지 피브티(Nureca Technologies Pvt)가 표준 인증기관 인터텍(Intertek)으로부터 획득했다.이번 국제표준 인증은 인도에서 의료기기 제조 공장에 대한 주요 이정표를 나타내는 것으로 분석된다. 인증이 헬스케어 업계에서 품질 및 규정 준수에 대한 약속으로 평가받기 때문이다.ISO 13485는 프로세스의 효율성을 설정하고 유지하는 품질관리시스템(QMS)에서 의료기기 제조업체를 지원하기 위해 작성됐다. 특히 안전한 의료기기의 폐기까지 일관된 설계, 개발, 생산, 설치 및 배송을 보장한다.누레카는 대표 브랜드 "닥터트러스트(DR Trust)"를 보유한 디지털 헬스케어 선도기업이다. 닥터트러스트 제품은 미국 식품의약국(USFDA) 및 CE와 같은 글로벌 표준도 준수한다.특히 닥터트러스트 360 플랫폼은 독립형 제품에서 스마트 장치, 소프트웨어 및 시스템을 결합한 솔루션으로 전환을 주도하고 있다.뉴레카는 데이터 과학 기능을 활용해 만성 병을 앓고 있는 많은 사람들이 더 건강하고 나은 삶을 살 수 있도록 지원하고 있다.
[인도] 뉴레카, 분무기 및 혈압 모니터에 국제표준 ISO 13485:2016 인증 획득인도 헬스케어 기업인 뉴레카(Nureca)에 따르면 분무기 및 혈압 모니터에 대해 국제표준 ISO 13485:2016 인증을 획득했다. ISO 13485:2016 표준은 의료기기 품질경영시스템과 관련돼 있다.인증은 뉴레카가 전액 출자한 자회사인 뉴레카테크놀로지 피브티(Nureca Technologies Pvt)가 표준 인증기관 인터텍(Intertek)으로부터 획득했다.이번 국제표준 인증은 인도에서 의료기기 제조 공장에 대한 주요 이정표를 나타내는 것으로 분석된다. 인증이 헬스케어 업계에서 품질 및 규정 준수에 대한 약속으로 평가받기 때문이다.ISO 13485는 프로세스의 효율성을 설정하고 유지하는 품질관리시스템(QMS)에서 의료기기 제조업체를 지원하기 위해 작성됐다. 특히 안전한 의료기기의 폐기까지 일관된 설계, 개발, 생산, 설치 및 배송을 보장한다.누레카는 대표 브랜드 "닥터트러스트(DR Trust)"를 보유한 디지털 헬스케어 선도기업이다. 닥터트러스트 제품은 미국 식품의약국(USFDA) 및 CE와 같은 글로벌 표준도 준수한다.특히 닥터트러스트 360 플랫폼은 독립형 제품에서 스마트 장치, 소프트웨어 및 시스템을 결합한 솔루션으로 전환을 주도하고 있다.뉴레카는 데이터 과학 기능을 활용해 만성 병을 앓고 있는 많은 사람들이 더 건강하고 나은 삶을 살 수 있도록 지원하고 있다. -
![[미국] 일리노이주, PFAS로 존재하는 위협 문제를 해결하기 위해 새로운 규칙과 법률 제안](http://stdnews.kr/data/file/news/thumb/thumb-2944253047_B2pl0Yfb_94e087eef32067dd50bf6ecd56f2936ebf8be9e2_200x180.jpg) [미국] 일리노이주, PFAS로 존재하는 위협 문제를 해결하기 위해 새로운 규칙과 법률 제안미국 일리노이주는 영원한 화학물질 PFAS(per-and polyfluoroalkyl substances)로 존재하는 위협 문제를 해결하기 위해 새로운 규칙과 법률을 제안했다.2022년 1월 1일 PFAS를 함유한 Class B 소방용 발포제의 제조, 판매, 판매를 위한 유통, 사용을 위한 유통 등을 금지하는 법률이 발효됐다.또한 일리노이주는 5가지 PFAS 화학물질에 대한 지하수 품질 표준을 정하는 규칙을 제안했다. 지하수 기준은 미국 EPA에서 발표한 건강 기준 표준보다 매우 엄격하다.과불화화합물(폴리플루오르화 알킬 물질) PFAS는 광범위한 소비자 및 산업 제품에 사용되는 다양한 인공 화학 물질 그룹이다.일부 PFAS는 다른 것에 비해 더욱 광범위하게 사용되고 있으며 연구도 진행 중이다. 많은 PFAS는 그리스, 오일, 물, 열에 저항을 갖고 있다.이러한 특징에 의해 지난 1940년부터 얼룩, 방수 직물, 카페트, 청소 제품, 페인트, 소방용 발포체 등 다양한 용도로 사용됐다. 특정 PFAS는 조리기구, 식품 포장, 식품 가공 장비 등에 제한적으로 사용하도록 FDA 승인을 받기도 했다.최근 혈액 검사를 통해 PFAS가 사람과 동물에게 축적된다는 사실이 밝혀졌다. 생물학적 축적이 건강에 심각한 상태를 유발할 수 있는 것으로 밝혀졌다. 주 정부와 연방 EPA는 화학 물질에 대한 토양 및 지하수 정화 목표 수준을 설정하기 위해 빠르게 움직이고 있다.FDA는 국립보건원, 질병통제 예방센터, 환경보호청, 농무부, 국방부, 일리노이주 및 지역 파트너와 PFAS노출 경로를 파악하고 관련 건강 위험을 이해하고 위험에 대한 대중 노출을 줄이기 위해 지속적으로 일하고 있다.
[미국] 일리노이주, PFAS로 존재하는 위협 문제를 해결하기 위해 새로운 규칙과 법률 제안미국 일리노이주는 영원한 화학물질 PFAS(per-and polyfluoroalkyl substances)로 존재하는 위협 문제를 해결하기 위해 새로운 규칙과 법률을 제안했다.2022년 1월 1일 PFAS를 함유한 Class B 소방용 발포제의 제조, 판매, 판매를 위한 유통, 사용을 위한 유통 등을 금지하는 법률이 발효됐다.또한 일리노이주는 5가지 PFAS 화학물질에 대한 지하수 품질 표준을 정하는 규칙을 제안했다. 지하수 기준은 미국 EPA에서 발표한 건강 기준 표준보다 매우 엄격하다.과불화화합물(폴리플루오르화 알킬 물질) PFAS는 광범위한 소비자 및 산업 제품에 사용되는 다양한 인공 화학 물질 그룹이다.일부 PFAS는 다른 것에 비해 더욱 광범위하게 사용되고 있으며 연구도 진행 중이다. 많은 PFAS는 그리스, 오일, 물, 열에 저항을 갖고 있다.이러한 특징에 의해 지난 1940년부터 얼룩, 방수 직물, 카페트, 청소 제품, 페인트, 소방용 발포체 등 다양한 용도로 사용됐다. 특정 PFAS는 조리기구, 식품 포장, 식품 가공 장비 등에 제한적으로 사용하도록 FDA 승인을 받기도 했다.최근 혈액 검사를 통해 PFAS가 사람과 동물에게 축적된다는 사실이 밝혀졌다. 생물학적 축적이 건강에 심각한 상태를 유발할 수 있는 것으로 밝혀졌다. 주 정부와 연방 EPA는 화학 물질에 대한 토양 및 지하수 정화 목표 수준을 설정하기 위해 빠르게 움직이고 있다.FDA는 국립보건원, 질병통제 예방센터, 환경보호청, 농무부, 국방부, 일리노이주 및 지역 파트너와 PFAS노출 경로를 파악하고 관련 건강 위험을 이해하고 위험에 대한 대중 노출을 줄이기 위해 지속적으로 일하고 있다. -
![[캐나다] 스파이나FX 메디컬(SpinaFX Medical), QMS 및 MDSAP 인증 획득](http://stdnews.kr/data/file/news/thumb/thumb-2949739381_oHuPrXp1_1b14781364dc8e7cdb185f76254c56b22d4cff1a_200x180.jpg) [캐나다] 스파이나FX 메디컬(SpinaFX Medical), QMS 및 MDSAP 인증 획득▲컴퓨터 제어 콘솔, 일회용 주사기 및 멸균 케이스를 포함한 오존발생챔버 등 트리오젝션 시스템 [출처=홈페이지] 캐나다 스파이나FX 메디컬(SpinaFX Medical)은 자사 트리오젝션 시스템(Triojection system)의 품질관리시스템(quality management system, QMS)이 미국과 캐나다에서 ISO 13485:2016 인증을 획득했다고 밝혔다.또한 미국과 캐나다에서 의료장비 단일 심사 프로그램(Medical Device Single Audit Program, MDSAP) 인증을 받았으며 유럽에서 EN ISO 13485:2016 인증을 획득했다.스파이나FX의 ISO 및 MDSAP 인증은 독립적인 제3자 인증업체인 인터텍(Intertek Group)에서 진행했다. 인증획득으로 새로운 이정표를 쓰게 된 것이다.인증을 획득한 것은 스파이나FX 팀과 계약 제조기업 스타피시 메디컬(Starfish Medical)의 고품질, 교차 기능, 협력적인 노력의 결과이다.스파이나FX의 ISO/MDSAP 인증은 캐나다 보건부, EU MDR, 미국 FDA 등 의료기기 라이선스 및 승인을 추구할 수 있는 중요한 전제 조건이 된다.ISO 13485:2016은 의료기기의 품질관리시스템에 대한 일련의 요구 사항에 대해 국제적으로 인정받고 있는 표준이다. 고객 및 해당 규제 요구사항을 일관되게 충족하는 의료기기 및 관련 서비스를 제공할 수 있는 능력을 입증해야 된다.스파이나FX는 최소 침습 영상 유도 치료 솔루션 및 기술 기업으로 캐나다 온타리오주 콩고드에 위치하고 있다. 마지막으로 펀딩을 받은 것은 2021년 11월1일 시리즈 A라운드다.
[캐나다] 스파이나FX 메디컬(SpinaFX Medical), QMS 및 MDSAP 인증 획득▲컴퓨터 제어 콘솔, 일회용 주사기 및 멸균 케이스를 포함한 오존발생챔버 등 트리오젝션 시스템 [출처=홈페이지] 캐나다 스파이나FX 메디컬(SpinaFX Medical)은 자사 트리오젝션 시스템(Triojection system)의 품질관리시스템(quality management system, QMS)이 미국과 캐나다에서 ISO 13485:2016 인증을 획득했다고 밝혔다.또한 미국과 캐나다에서 의료장비 단일 심사 프로그램(Medical Device Single Audit Program, MDSAP) 인증을 받았으며 유럽에서 EN ISO 13485:2016 인증을 획득했다.스파이나FX의 ISO 및 MDSAP 인증은 독립적인 제3자 인증업체인 인터텍(Intertek Group)에서 진행했다. 인증획득으로 새로운 이정표를 쓰게 된 것이다.인증을 획득한 것은 스파이나FX 팀과 계약 제조기업 스타피시 메디컬(Starfish Medical)의 고품질, 교차 기능, 협력적인 노력의 결과이다.스파이나FX의 ISO/MDSAP 인증은 캐나다 보건부, EU MDR, 미국 FDA 등 의료기기 라이선스 및 승인을 추구할 수 있는 중요한 전제 조건이 된다.ISO 13485:2016은 의료기기의 품질관리시스템에 대한 일련의 요구 사항에 대해 국제적으로 인정받고 있는 표준이다. 고객 및 해당 규제 요구사항을 일관되게 충족하는 의료기기 및 관련 서비스를 제공할 수 있는 능력을 입증해야 된다.스파이나FX는 최소 침습 영상 유도 치료 솔루션 및 기술 기업으로 캐나다 온타리오주 콩고드에 위치하고 있다. 마지막으로 펀딩을 받은 것은 2021년 11월1일 시리즈 A라운드다.


![[특집-ISO/IEC JTC 1/SC 17 활동] 35. Result of voting on SR Ballot for ISO/](http://stdnews.kr/data/file/news/thumb/thumb-3555379571_4cufp2BH_756bcefa64e6169e58646ad7b061ecbec455fb11_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 34. Result of voting on SR ballot for ISO/](http://stdnews.kr/data/file/news/thumb/thumb-3555380113_kIQxAlfN_727cc6e35ccb9d5e6c07574a3b3a2ab9db104d48_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 33. Result of voting on SR ballot for ISO/](http://stdnews.kr/data/file/news/thumb/thumb-32068165_R52GPIij_2bca2660198a937d2534db7bfd9fc8174a76cfa2_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 32. Result of voting on SR Ballot for ISO/](http://stdnews.kr/data/file/news/thumb/thumb-32068165_TxRrtYEa_c36d1a53acc15db7e18fae132ffef64e11bda43c_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 31. Result of voting on SR Ballot for ISO/](http://stdnews.kr/data/file/news/thumb/thumb-3555377690_nrjmWhSf_d9b63299e7f3f52053141cae28f32f7df40b5918_340x240.jpg)


![[일본] 요코하마(横浜), 3월 원격근무로 일하는 50대 여성이 장시간 노동을 강요받아 적응장애가 발병해 산재로 인정받아](http://stdnews.kr/data/file/news/thumb/thumb-3555377672_BapV2SmF_41a011a26290be1daa3f6a5220df7b8b6d167f69_340x240.jpg)
![[인도] 마하라슈트라주 식품의약국(Maharashtra FDA), 맥도날드 상품명에 치즈를 잘못 표기해 소비자 기만 지적](http://stdnews.kr/data/file/news/thumb/thumb-3743818281_Uu5GpcKZ_6890f33f4b087f58686ed20e46a04bbb79ad883e_340x240.jpg)
![[남아공] 토코만 푸드(Thokoman Foods), 자사 땅콩버터 식품 안전성 재확인](http://stdnews.kr/data/file/news/thumb/thumb-3743818281_h5HrK0kT_c2453abdb4577a16b34590f5b8f76de9c2a95469_340x240.jpg)
![[일본] 혼다(ホンダ), 2030년까지 전기자동차(EV)를 중심으로 하는 전동화와 소트프웨어 개발에 10조 엔을 투자할 계획](http://stdnews.kr/data/file/news/thumb/thumb-3555381172_1g5z7YDN_4db7699b271b5e9dbbe1a4f6dc69fb01a9881abb_340x240.jpg)
![[일본] 자민당(自民党), 기업이 직원을 고객의 '카스하라(カスハラ)로부터 보호를 의무로 하는 방안을 고려 중](http://stdnews.kr/data/file/news/thumb/thumb-3555381172_PCNyaL1v_9f9b79d526b4be07024401e874fe26f618a42e7c_340x240.jpg)
![[일본] 총무성(総務省), 2023년 기준 전국의 빈집은 900만 호로 사상 최고치 기록](http://stdnews.kr/data/file/news/thumb/thumb-3555379571_qr01mWC9_fef7fa874e596585a04ee2dae235376595341779_340x240.jpg)
![[특집-기상기후재난] 한국중부발전(주) 신정철 선임 인터뷰 - 행정안전부 뿐 아니라 기상기후 연계조직 모두가 참여하는 협의체가](http://stdnews.kr/data/file/news/thumb/thumb-3555374516_iKWwUBas_9c1729f1e3977ee50c398986e7f98d5002a57deb_340x240.jpg)
![[특집-기상기후재난] (주)비밍코어 정성민 대표 인터뷰 - 인공지능(AI) 활용한 기후재난 대처 솔루션 개발](http://stdnews.kr/data/file/news/thumb/thumb-3555374391_0JZYhIcj_dca23c54fc7923952082a9d7af92db00b9dd33c9_340x240.jpg)
![[기획-표준 전문가] 한국투자증권 김범수 FC 인터뷰 - 표준전문가 양성 교육이 지속되길 희망](http://stdnews.kr/data/file/news/thumb/thumb-3555374114_Np9hM7aC_e6ffa916aade15e1c301badf3132ed3f0551a900_340x240.jpg)
![[특집-기상기후재난] 행정안전부 안전교육 전문인력 유정희 강사 인터뷰 - 기상기후재난예방 전문가 양성 시급](http://stdnews.kr/data/file/news/thumb/thumb-3555374240_gOmdLG10_cfc17ed887dccc93f503013bf794ed568a5d40dc_340x240.jpg)
![[특집-기상기후재난] (주)이토스 김형식 대표 인터뷰 - 재난을 사전에 예측·예방할 기술개발 시급](http://stdnews.kr/data/file/news/thumb/thumb-32068165_lmUrCBIn_797dc8926bb7d90542546463cc73e6233f0bbb46_340x240.png)