검색결과
-
 해썹인증원, ‘해썹 코리아(HACCP KOREA) 2023’ 개최한국식품안전관리인증원(해썹인증원)은 서울 코엑스(COEX)에서 22일에 개최한 ‘해썹 코리아(HACCP KOREA) 2023’과 22일부터 25일까지 ‘해썹 홍보관’과 ‘스마트 해썹 기획관’ 등을 운영했다고 28일 밝혔다. 이번 행사는 국내 유일 해썹 종합행사로 국내외 식품안전 전문가가 한자리에 모여 기술정보를 교류했다. 또한 체험하고 즐기면서 ‘해썹’과 ‘스마트 해썹’을 보다 쉽게 이해할 수 있도록 했다. 한상배 원장은 개회사를 통해 “‘해썹 코리아 2023’을 통해 식품안전의 현재와 미래를 만나는 유익한 계기가 되길 바란다”며 “한국식품안전관리인증원은 변화하는 식품 트렌드와 환경에 맞춰 우리 사회의 안전한 먹거리를 위해 한 단계 더 도약할 수 있도록 노력하겠다”고 말했다. 개회식과 시상식이 진행된 1부에서는 ‘안전관리인증기준(HACCP) 짧은 영상(숏폼) 공모전’ 대상, ‘해썹 발전 유공자’ 10명이 식약처장 표창을 수상했으며 20개 업체가 ‘해썹 우수영업장’으로 선정돼 해썹인증원장상을 수상했다. 또한 ‘SNS 우수 서포터즈’(3점), ‘스마트 해썹 데이터 활용 경진대회’(6점) 수상자에 대한 시상을 진행했다. 정책포럼이 진행된 2부에서는 ‘스마트 해썹 전환에 따른 식품안전관리 미래 전략’을 주제로 해썹인증원 서연범 기술혁신본부장이 ‘데이터 기반의 업체 맞춤형 해썹 케어 서비스’를, 풀무원 오승훈 SCM기획실장이 ‘식품 안전 및 신뢰성 강화를 위한 Digital Trust Ecosystem’를, 식품안전정보원 정책연구실장 이주형 실장이 ‘식품안전관리 패러다임 변화에 따른 해썹의 현재와 미래’를 발표했다. 이어 주제발표 연사를 포함하여 식품의약품안전처 손영욱 과장, 순천대학교 김중범 교수가 참석해 패널토론 및 질의응답도 진행됐다. 3부 국제세미나에서는 미국 식품의약국(FDA), 일본 식품안전관리협회(JFSM) 등 2개국 3명의 전문가가 연사로 나서 ‘수출국 식품안전관리 동향 및 대응 전략’을 주제로 발표해 수출업체의 애로사항을 해소했다. ‘해썹 코리아 2023’에 참여한 A업체 관계자는 “시상식을 통해 우수한 식품안전관리로 안전한 제품을 생산하는 업체를 알게 됐다”며 “이번 행사를 통해 스마트 해썹의 현재와 미래에 대해 이해하고 국내외 식품안전 전문가를 만나볼 수 있는 유익한 시간이었다”고 소감을 말했다. 또한 ‘해썹 홍보관’과 ‘스마트 해썹 기획관’에서 ‘해썹 스탬프 도장 깨기 이벤트’, ‘해썹과 인생네컷’, ‘7원칙 스톱워치 게임’, ‘OX 퀴즈’ 등 다양한 게임을 통해 기념품을 증정하고 산업체의 참여 기회를 넓혀 해썹과 스마트 해썹에 대한 적극적인 홍보를 진행하여 참관객들의 참여도를 높였다. ‘해썹 코리아 2023’ 행사영상은 식약처와 해썹인증원 유튜브 채널(#식품의약품안전처, #한국식품안전관리인증원)에서 지속 시청 가능하며 발표자료는 누리집(www.haccp.or.kr)에서 확인할 수 있다.
해썹인증원, ‘해썹 코리아(HACCP KOREA) 2023’ 개최한국식품안전관리인증원(해썹인증원)은 서울 코엑스(COEX)에서 22일에 개최한 ‘해썹 코리아(HACCP KOREA) 2023’과 22일부터 25일까지 ‘해썹 홍보관’과 ‘스마트 해썹 기획관’ 등을 운영했다고 28일 밝혔다. 이번 행사는 국내 유일 해썹 종합행사로 국내외 식품안전 전문가가 한자리에 모여 기술정보를 교류했다. 또한 체험하고 즐기면서 ‘해썹’과 ‘스마트 해썹’을 보다 쉽게 이해할 수 있도록 했다. 한상배 원장은 개회사를 통해 “‘해썹 코리아 2023’을 통해 식품안전의 현재와 미래를 만나는 유익한 계기가 되길 바란다”며 “한국식품안전관리인증원은 변화하는 식품 트렌드와 환경에 맞춰 우리 사회의 안전한 먹거리를 위해 한 단계 더 도약할 수 있도록 노력하겠다”고 말했다. 개회식과 시상식이 진행된 1부에서는 ‘안전관리인증기준(HACCP) 짧은 영상(숏폼) 공모전’ 대상, ‘해썹 발전 유공자’ 10명이 식약처장 표창을 수상했으며 20개 업체가 ‘해썹 우수영업장’으로 선정돼 해썹인증원장상을 수상했다. 또한 ‘SNS 우수 서포터즈’(3점), ‘스마트 해썹 데이터 활용 경진대회’(6점) 수상자에 대한 시상을 진행했다. 정책포럼이 진행된 2부에서는 ‘스마트 해썹 전환에 따른 식품안전관리 미래 전략’을 주제로 해썹인증원 서연범 기술혁신본부장이 ‘데이터 기반의 업체 맞춤형 해썹 케어 서비스’를, 풀무원 오승훈 SCM기획실장이 ‘식품 안전 및 신뢰성 강화를 위한 Digital Trust Ecosystem’를, 식품안전정보원 정책연구실장 이주형 실장이 ‘식품안전관리 패러다임 변화에 따른 해썹의 현재와 미래’를 발표했다. 이어 주제발표 연사를 포함하여 식품의약품안전처 손영욱 과장, 순천대학교 김중범 교수가 참석해 패널토론 및 질의응답도 진행됐다. 3부 국제세미나에서는 미국 식품의약국(FDA), 일본 식품안전관리협회(JFSM) 등 2개국 3명의 전문가가 연사로 나서 ‘수출국 식품안전관리 동향 및 대응 전략’을 주제로 발표해 수출업체의 애로사항을 해소했다. ‘해썹 코리아 2023’에 참여한 A업체 관계자는 “시상식을 통해 우수한 식품안전관리로 안전한 제품을 생산하는 업체를 알게 됐다”며 “이번 행사를 통해 스마트 해썹의 현재와 미래에 대해 이해하고 국내외 식품안전 전문가를 만나볼 수 있는 유익한 시간이었다”고 소감을 말했다. 또한 ‘해썹 홍보관’과 ‘스마트 해썹 기획관’에서 ‘해썹 스탬프 도장 깨기 이벤트’, ‘해썹과 인생네컷’, ‘7원칙 스톱워치 게임’, ‘OX 퀴즈’ 등 다양한 게임을 통해 기념품을 증정하고 산업체의 참여 기회를 넓혀 해썹과 스마트 해썹에 대한 적극적인 홍보를 진행하여 참관객들의 참여도를 높였다. ‘해썹 코리아 2023’ 행사영상은 식약처와 해썹인증원 유튜브 채널(#식품의약품안전처, #한국식품안전관리인증원)에서 지속 시청 가능하며 발표자료는 누리집(www.haccp.or.kr)에서 확인할 수 있다. -
 식약처, 첨단바이오의약품 개발 지원 위한 가이드라인 제·개정식품의약품안전처는 첨단바이오의약품의 개발을 지원하기 위한 가이드라인 2종을 제정 및 개정 하고 임상시험 신청 시 자료 준비에 도움을 줄 수 있도록 하는 규제과학 상담사례집을 발간했다고 밝혔다. 이번 가이드라인 제·개정이 우수한 첨단바이오의약품의 개발을 지원하고 합리적인 품질관리를 수행하는 데 도움을 줄 것으로 기대된다. 첫째, ‘개인 맞춤형 신생항원 치료제 개발시 고려사항’을 제정했다. 최근 환자 개인의 신생항원을 사용한 항암제 개발이 증가함에 따라 치료제개발 시 필요한 고려사항을 안내하는 가이드라인을 선제적으로 마련했다. 신생항원이란 암세포의 DNA에 특정 돌연변이가 발생해 정상세포에서는 발현하지 않고 암세포에서만 선별적으로 발현하는 새로운 단백질을 의미한다. 기존 항암제와 달리 개인별 맞춤형으로 제조되는 특성을 반영하여 종양조직 채취부터 신생항원 제조까지 품질평가 방법, 비임상및임상 시험 시 고려사항 등을 제시했다. 둘째, ‘세포치료제 세포은행 평가 민원인 안내서’를 개정했다. 세포치료제는 소규모로 제조되기 때문에 세포은행을 자주 구축 및 변경해야 하는 어려움이 있으므로 세포은행 구축 의무 대상을 명확하게 제시하여 개발자의 부담을 줄이기 위해 관련 가이드라인을 개정했다. 세포은행은 특성이 규명된 세포를 동일한 조건에서 배양하여 얻은 균질한 세포를 여러 개의 용기에 같은 양으로 나눠 담고 정해진 조건에서 보관하는 것으로 제조의 일관성을 확보하기 위해 운영한다. 세포원액 품질관리 기준 적절성 등 과학적 근거와 해외 사례를 기반으로 제조 규모가 작은 세포치료제의 경우 세포은행 구축에 대한 예외를 적용받도록 했다. 아울러 1인의 기증자로부터 소량의 완제의약품을 생산할 경우 세포은행을구축하는 대신 기증자간 동등성 평가 등 과학적 근거를 통해 세포원액으로설정하여 품질관리 하도록 하고 그 타당성과 변경 관리계획에 대해서는식약처와 사전에 협의하도록 했다. 셋째, ‘첨단바이오의약품 규제과학 상담사례집’을 발간했다. 첨단바이오의약품의 신속한 임상시험을 지원하기 위해 신청 시 제출해야 하는 자료 관련 질의와 답변, 그리고 다양한 상담 사례를 구체적으로 안내했다. 식약처 관계자는 “이번 안내서 제·개정이 우수한 첨단바이오의약품의 개발을 지원하고 합리적인 품질관리를 수행하는 데 도움을 줄 것으로 기대한다”며 “앞으로도 전문성과 규제과학을 바탕으로 첨단바이오의약품의 제품화를 적극지원하도록 노력할 계획”이라고 밝혔다. 자세한 내용은 ‘식약처 누리집(mfds.go.kr) > 법령/자료 > 자료실 > 안내서/지침’에서 확인할 수 있다.
식약처, 첨단바이오의약품 개발 지원 위한 가이드라인 제·개정식품의약품안전처는 첨단바이오의약품의 개발을 지원하기 위한 가이드라인 2종을 제정 및 개정 하고 임상시험 신청 시 자료 준비에 도움을 줄 수 있도록 하는 규제과학 상담사례집을 발간했다고 밝혔다. 이번 가이드라인 제·개정이 우수한 첨단바이오의약품의 개발을 지원하고 합리적인 품질관리를 수행하는 데 도움을 줄 것으로 기대된다. 첫째, ‘개인 맞춤형 신생항원 치료제 개발시 고려사항’을 제정했다. 최근 환자 개인의 신생항원을 사용한 항암제 개발이 증가함에 따라 치료제개발 시 필요한 고려사항을 안내하는 가이드라인을 선제적으로 마련했다. 신생항원이란 암세포의 DNA에 특정 돌연변이가 발생해 정상세포에서는 발현하지 않고 암세포에서만 선별적으로 발현하는 새로운 단백질을 의미한다. 기존 항암제와 달리 개인별 맞춤형으로 제조되는 특성을 반영하여 종양조직 채취부터 신생항원 제조까지 품질평가 방법, 비임상및임상 시험 시 고려사항 등을 제시했다. 둘째, ‘세포치료제 세포은행 평가 민원인 안내서’를 개정했다. 세포치료제는 소규모로 제조되기 때문에 세포은행을 자주 구축 및 변경해야 하는 어려움이 있으므로 세포은행 구축 의무 대상을 명확하게 제시하여 개발자의 부담을 줄이기 위해 관련 가이드라인을 개정했다. 세포은행은 특성이 규명된 세포를 동일한 조건에서 배양하여 얻은 균질한 세포를 여러 개의 용기에 같은 양으로 나눠 담고 정해진 조건에서 보관하는 것으로 제조의 일관성을 확보하기 위해 운영한다. 세포원액 품질관리 기준 적절성 등 과학적 근거와 해외 사례를 기반으로 제조 규모가 작은 세포치료제의 경우 세포은행 구축에 대한 예외를 적용받도록 했다. 아울러 1인의 기증자로부터 소량의 완제의약품을 생산할 경우 세포은행을구축하는 대신 기증자간 동등성 평가 등 과학적 근거를 통해 세포원액으로설정하여 품질관리 하도록 하고 그 타당성과 변경 관리계획에 대해서는식약처와 사전에 협의하도록 했다. 셋째, ‘첨단바이오의약품 규제과학 상담사례집’을 발간했다. 첨단바이오의약품의 신속한 임상시험을 지원하기 위해 신청 시 제출해야 하는 자료 관련 질의와 답변, 그리고 다양한 상담 사례를 구체적으로 안내했다. 식약처 관계자는 “이번 안내서 제·개정이 우수한 첨단바이오의약품의 개발을 지원하고 합리적인 품질관리를 수행하는 데 도움을 줄 것으로 기대한다”며 “앞으로도 전문성과 규제과학을 바탕으로 첨단바이오의약품의 제품화를 적극지원하도록 노력할 계획”이라고 밝혔다. 자세한 내용은 ‘식약처 누리집(mfds.go.kr) > 법령/자료 > 자료실 > 안내서/지침’에서 확인할 수 있다. -
 의료기기 국제 규제 선도 및 수출 지원한다식품의약품안전처는 우리나라 의료기기 규제 체계를 널리 알리고국산 의료기기의 수출지원 방안을 모색하기 위해 중국 상하이에서 개최되는 제27차 국제의료기기규제조화회의 연례총회(GHWP Annual meeting)에 27일부터 30일까지 참석한다고 밝혔다. GHWP(Global Harmonization Working Party)는 의료기기 국제 규제조화를 위해 1996년 발족한 협력 기구로 현재 미국, 일본, 중국, 싱가포르 등 세계 33개 회원국이 참여하며 기술위원회(Technical Committee)와 8개실무그룹(Working Group)이 운영된다. 국내 규제역량을 기반으로 국제 협력을 주도하고 규제기관 간 네트워크를 강화해 국내 우수한 제품이 세계 시장에서 인정받고 원활하게 수출될 전망이다. 식약처는 그간 전문성을 인정받아 2015년부터 2017년까지GHWP 의장국으로활동했으며 현재 GHWP 내 전략자문단과 실무그룹1(WG1)에서 의장직을 맡아 글로벌 규제 조화를 통한 국산 제품의 세계 시장 진출을 적극 지원하고 있다. 식약처는 이번 회의에서 인공지능 의료기기 규제사례, 혁신의료기기 규제 방향, 우리나라 선진 규제 체계 등에 대해 발표하고 우리나라의 규제과학 우수성과 혁신의료기기의 신속한 시장진입 성과를 알릴 계획이다. 또한 30일 연례총회에서 식약처 주도로 개정한 국제공통가이드라인 3건의승인을 요청할 예정이다. 더불어 식약처는 총회에 참석한 각국 규제당국과 양자 협력 회의를 통해 디지털 헬스분야 협력 방안을 모색할 계획이다. 식약처 관계자는 “앞으로도 우수한 규제역량을 기반으로 국제 협력을 주도하고 규제기관 간 네트워크를 강화해 우리의 우수한 제품이 세계 시장에서 인정받고 원활하게 수출될 수 있도록 최선을 다해 지원할 계획”이라고 밝혔다.
의료기기 국제 규제 선도 및 수출 지원한다식품의약품안전처는 우리나라 의료기기 규제 체계를 널리 알리고국산 의료기기의 수출지원 방안을 모색하기 위해 중국 상하이에서 개최되는 제27차 국제의료기기규제조화회의 연례총회(GHWP Annual meeting)에 27일부터 30일까지 참석한다고 밝혔다. GHWP(Global Harmonization Working Party)는 의료기기 국제 규제조화를 위해 1996년 발족한 협력 기구로 현재 미국, 일본, 중국, 싱가포르 등 세계 33개 회원국이 참여하며 기술위원회(Technical Committee)와 8개실무그룹(Working Group)이 운영된다. 국내 규제역량을 기반으로 국제 협력을 주도하고 규제기관 간 네트워크를 강화해 국내 우수한 제품이 세계 시장에서 인정받고 원활하게 수출될 전망이다. 식약처는 그간 전문성을 인정받아 2015년부터 2017년까지GHWP 의장국으로활동했으며 현재 GHWP 내 전략자문단과 실무그룹1(WG1)에서 의장직을 맡아 글로벌 규제 조화를 통한 국산 제품의 세계 시장 진출을 적극 지원하고 있다. 식약처는 이번 회의에서 인공지능 의료기기 규제사례, 혁신의료기기 규제 방향, 우리나라 선진 규제 체계 등에 대해 발표하고 우리나라의 규제과학 우수성과 혁신의료기기의 신속한 시장진입 성과를 알릴 계획이다. 또한 30일 연례총회에서 식약처 주도로 개정한 국제공통가이드라인 3건의승인을 요청할 예정이다. 더불어 식약처는 총회에 참석한 각국 규제당국과 양자 협력 회의를 통해 디지털 헬스분야 협력 방안을 모색할 계획이다. 식약처 관계자는 “앞으로도 우수한 규제역량을 기반으로 국제 협력을 주도하고 규제기관 간 네트워크를 강화해 우리의 우수한 제품이 세계 시장에서 인정받고 원활하게 수출될 수 있도록 최선을 다해 지원할 계획”이라고 밝혔다. -
 식약처, ‘대체식품 표시 가이드라인’ 배포해 식품산업 활성화 지원한다식품의약품안전처는 식물성 원료 등을 사용해 동물성 식품과 유사하게 만든 ‘대체식품’을 제품에 표시하려는 영업자가 준수해야 하는 기준과 방법을 제시하는 '대체식품의 표시 가이드라인'을 마련및배포한다고 27일 밝혔다. 이에 대체식품에 대한 정확한 정보제공으로 소비자의 오인 및 혼동을 방지하고 다양한 대체식품 표시가 가능해져 미래 먹거리산업 경쟁력이 강화될 것으로 기대된다. 대체식품이란 동물성 원료 대신 식물성 원료, 미생물, 식용곤충, 세포배양물 등을 주원료로 사용해 기존 식품과 유사한 형태, 맛, 조직감 등을 가지도록 제조했다는 것을 표시해 판매하는 식품을 말한다. 식약처는 이번 가이드라인이 대체식품에 대한 소비자의 관심이 높아지고 세계적으로관련 시장이 급성장함에 따라 대체식품의 특성을 설명할 수 있는 표시‧광고를 가능하게 함으로써 관련 업계의 다양한 제품 개발을 지원하는 한편소비자의 알권리와 선택권을 보장하기 위해 마련됐다고 설명했다. 가이드라인의 적용범위는 대체식품을 제조‧가공‧수입‧소분하는 영업자가 대체식품의 용기 또는 포장에 대체식품임을 표시하는 경우에 적용한다. 표시해야 하는 항목에는 대체식품의 주표시면에 ‘대체식품’임을 명확히 알리는 ▲‘대체식품’ 용어 ▲동물성 식품 등으로 오인‧혼동하지 않도록하는 제품명 ▲동물성 원료의 포함 여부 등 3가지를 모두 표시해야 한다. 주표시면은 용기‧포장의 표시면 중 상표, 로고 등이 인쇄되어 있어 소비자가 식품 또는 식품첨가물을 구매할 때 통상적으로 볼 수 있는 면을 말한다. 대체식품에 표시해야 하는 3가지 항목의 세부표시방법은 다음과 같다. ‘대체식품’이라는 용어는 소비자가 쉽게 확인할 수 있도록 14pt 이상의 글씨로 표시해야 한다. 제품명은 ‘식물성 제품’임을 강조하거나 대체한 원재료의 명칭을 포함한 경우에 한해 불고기, 함박스테이크 등 동물성 식품에 사용되는 요리명 등은사용할 수 있도록 허용했다. 다만 오해를 피하기 위해 ‘소고기’, ‘돼지고기’, ‘우유’, ‘계란’ 등의 1차 산물의 명칭은 대체식품의 제품명에 사용할 수 없다. 아울러 동물성 원료가 들어있지 않은 사실을 12pt 이상의 글씨로 표시해야 한다. 다만 식품 제조에 사용된 소스나 조미료 등에 동물성 원료가 미량 들어있는 경우에는 그 사실을 동일한 크기로 표시해야 한다. 참고로 ‘대체식품의 표시 가이드라인’을 준수하는 경우에 한해 현재 부당한 표시‧광고로 금지하고 있는다른 식품유형의 명칭(예: 소시지, 햄 등)을 사용하거나 사용하지 않은 원재료를 강조(예: MEAT FREE 등)하는 표시‧광고를예외적으로 사용할 수 있도록 했다. 식약처 관계자는 “소비자가 대체식품을 구매하는 경우 식품의 주표시면에 표시된 대체식품, 제품명, 동물성 원료 포함 여부 3가지를 확인하고 구매해야 한다”며 “앞으로도 소비자의 건강과 선택권 보장을 위한 정보 제공을 강화해 보다 안전한 식품 소비 환경이 조성되도록 노력하겠다”고 밝혔다. 가이드라인의 자세한 내용은 ‘식약처 대표 누리집(www.mfds.go.kr) → 법령/자료 → 법령정보 → 공무원지침서/민원인안내서’에서 확인할 수 있다.
식약처, ‘대체식품 표시 가이드라인’ 배포해 식품산업 활성화 지원한다식품의약품안전처는 식물성 원료 등을 사용해 동물성 식품과 유사하게 만든 ‘대체식품’을 제품에 표시하려는 영업자가 준수해야 하는 기준과 방법을 제시하는 '대체식품의 표시 가이드라인'을 마련및배포한다고 27일 밝혔다. 이에 대체식품에 대한 정확한 정보제공으로 소비자의 오인 및 혼동을 방지하고 다양한 대체식품 표시가 가능해져 미래 먹거리산업 경쟁력이 강화될 것으로 기대된다. 대체식품이란 동물성 원료 대신 식물성 원료, 미생물, 식용곤충, 세포배양물 등을 주원료로 사용해 기존 식품과 유사한 형태, 맛, 조직감 등을 가지도록 제조했다는 것을 표시해 판매하는 식품을 말한다. 식약처는 이번 가이드라인이 대체식품에 대한 소비자의 관심이 높아지고 세계적으로관련 시장이 급성장함에 따라 대체식품의 특성을 설명할 수 있는 표시‧광고를 가능하게 함으로써 관련 업계의 다양한 제품 개발을 지원하는 한편소비자의 알권리와 선택권을 보장하기 위해 마련됐다고 설명했다. 가이드라인의 적용범위는 대체식품을 제조‧가공‧수입‧소분하는 영업자가 대체식품의 용기 또는 포장에 대체식품임을 표시하는 경우에 적용한다. 표시해야 하는 항목에는 대체식품의 주표시면에 ‘대체식품’임을 명확히 알리는 ▲‘대체식품’ 용어 ▲동물성 식품 등으로 오인‧혼동하지 않도록하는 제품명 ▲동물성 원료의 포함 여부 등 3가지를 모두 표시해야 한다. 주표시면은 용기‧포장의 표시면 중 상표, 로고 등이 인쇄되어 있어 소비자가 식품 또는 식품첨가물을 구매할 때 통상적으로 볼 수 있는 면을 말한다. 대체식품에 표시해야 하는 3가지 항목의 세부표시방법은 다음과 같다. ‘대체식품’이라는 용어는 소비자가 쉽게 확인할 수 있도록 14pt 이상의 글씨로 표시해야 한다. 제품명은 ‘식물성 제품’임을 강조하거나 대체한 원재료의 명칭을 포함한 경우에 한해 불고기, 함박스테이크 등 동물성 식품에 사용되는 요리명 등은사용할 수 있도록 허용했다. 다만 오해를 피하기 위해 ‘소고기’, ‘돼지고기’, ‘우유’, ‘계란’ 등의 1차 산물의 명칭은 대체식품의 제품명에 사용할 수 없다. 아울러 동물성 원료가 들어있지 않은 사실을 12pt 이상의 글씨로 표시해야 한다. 다만 식품 제조에 사용된 소스나 조미료 등에 동물성 원료가 미량 들어있는 경우에는 그 사실을 동일한 크기로 표시해야 한다. 참고로 ‘대체식품의 표시 가이드라인’을 준수하는 경우에 한해 현재 부당한 표시‧광고로 금지하고 있는다른 식품유형의 명칭(예: 소시지, 햄 등)을 사용하거나 사용하지 않은 원재료를 강조(예: MEAT FREE 등)하는 표시‧광고를예외적으로 사용할 수 있도록 했다. 식약처 관계자는 “소비자가 대체식품을 구매하는 경우 식품의 주표시면에 표시된 대체식품, 제품명, 동물성 원료 포함 여부 3가지를 확인하고 구매해야 한다”며 “앞으로도 소비자의 건강과 선택권 보장을 위한 정보 제공을 강화해 보다 안전한 식품 소비 환경이 조성되도록 노력하겠다”고 밝혔다. 가이드라인의 자세한 내용은 ‘식약처 대표 누리집(www.mfds.go.kr) → 법령/자료 → 법령정보 → 공무원지침서/민원인안내서’에서 확인할 수 있다. -
 식약처, 의료기기 사이버보안을 위한 가이드라인 3종 배포식품의약품안전처는 유무선 통신 기능이 있는 의료기기의사이버보안 방안을 제시함으로써 안전한 의료기기 사용을 도모하기 위한 ‘의료기기 사이버보안 가이드라인’ 3종을 27일 발간·배포한다고 밝혔다. 이번 가이드라인이 의료기기 사이버 위협으로부터 환자 안전을 확보하는데 도움을 줄 것으로 기대된다. 사이버보안은 정보와 시스템이 무단 접근, 사용, 유출, 중단, 수정 또는 파괴와 같은 비인가 활동으로부터 보호돼 기밀성, 무결성, 가용성과 관련된 위험을 제품의 수명 주기 전체 동안 수용할 수 있는 수준으로 유지되는 상태를 말한다. 식약처가 27일 배포한 가이드라인 3종은 ‘의료기기 사이버보안 원칙 및 실무, ‘레거시 의료기기 사이버보안 원칙 및 실무’, ‘의료기기 사이버보안 위한 소프트웨어 자재명세서 원칙 및 실무’등이다. 가이드라인 3종의 주요 내용은 의료기기 사이버보안 보호 체계를 갖춘 제품의 개발과 사용 단계의 환자 보호,사이버 보안이 적용되지 않고 사용 중인의료기기를 위한 기업 및 의료기관의 역할, 의료기기 사이버보안 안전관리를 위한 소프트웨어 자재 명세서(SBOM) 수집과 정보 제공 방법 등이다. SBOM(Software Bill of Materials)은 소프트웨어를 구성하는 컴포넌트(소프트웨어 구성요소,펌웨어 등)와 컴포넌트 간 관계 등에 대한 정보 목록을 말한다. 식약처는 이번에 발간한 가이드라인 3종이 국제의료기기규제당국자포럼(IMDRF)에서2020년부터 올해까지 식약처 등 IMDRF 정회원이 마련한 총 3종의 의료기기 사이버보안국제 공통 가이드라인을 전문가의 검토를 거쳐 국내 업계에서 쉽게 참고할 수 있도록한글화하여 마련한 것이라고 설명했다. IMDRF는 의료기기 국제 규제조화를주도하는 미국·유럽 등 11개국 규제당국자 협의체로 우리나라는 2017년 12월에 가입했으며2021년에는 1년간 의장국을 맡아 수행했다. 식약처는 IMDRF 정회원으로서 동 국제 공통 가이드라인 마련을 위한 작업반에 적극 참여하고 있다. 식약처 관계자는 “소프트웨어 등디지털의료기기의 증가와 함께 사이버보안에대한위협도 증가하고 있다"며 "이번 가이드라인이 의료기기 사이버 위협으로부터 환자 안전을 확보하는데 도움을 줄 것으로 기대한다”고 전했다. 이어 “앞으로도 급변하는 디지털 환경에 신속히 대응하고 더욱 안전한 의료기기의 개발과 사용을 지원하기 위한 정보를 지속적으로 제공할 예정”이라고 덧붙였다. 자세한 내용은 ‘식약처 대표 누리집(mfds.go.kr)→법령/자료→법령정보→민원인안내서’에서 확인할 수 있다.
식약처, 의료기기 사이버보안을 위한 가이드라인 3종 배포식품의약품안전처는 유무선 통신 기능이 있는 의료기기의사이버보안 방안을 제시함으로써 안전한 의료기기 사용을 도모하기 위한 ‘의료기기 사이버보안 가이드라인’ 3종을 27일 발간·배포한다고 밝혔다. 이번 가이드라인이 의료기기 사이버 위협으로부터 환자 안전을 확보하는데 도움을 줄 것으로 기대된다. 사이버보안은 정보와 시스템이 무단 접근, 사용, 유출, 중단, 수정 또는 파괴와 같은 비인가 활동으로부터 보호돼 기밀성, 무결성, 가용성과 관련된 위험을 제품의 수명 주기 전체 동안 수용할 수 있는 수준으로 유지되는 상태를 말한다. 식약처가 27일 배포한 가이드라인 3종은 ‘의료기기 사이버보안 원칙 및 실무, ‘레거시 의료기기 사이버보안 원칙 및 실무’, ‘의료기기 사이버보안 위한 소프트웨어 자재명세서 원칙 및 실무’등이다. 가이드라인 3종의 주요 내용은 의료기기 사이버보안 보호 체계를 갖춘 제품의 개발과 사용 단계의 환자 보호,사이버 보안이 적용되지 않고 사용 중인의료기기를 위한 기업 및 의료기관의 역할, 의료기기 사이버보안 안전관리를 위한 소프트웨어 자재 명세서(SBOM) 수집과 정보 제공 방법 등이다. SBOM(Software Bill of Materials)은 소프트웨어를 구성하는 컴포넌트(소프트웨어 구성요소,펌웨어 등)와 컴포넌트 간 관계 등에 대한 정보 목록을 말한다. 식약처는 이번에 발간한 가이드라인 3종이 국제의료기기규제당국자포럼(IMDRF)에서2020년부터 올해까지 식약처 등 IMDRF 정회원이 마련한 총 3종의 의료기기 사이버보안국제 공통 가이드라인을 전문가의 검토를 거쳐 국내 업계에서 쉽게 참고할 수 있도록한글화하여 마련한 것이라고 설명했다. IMDRF는 의료기기 국제 규제조화를주도하는 미국·유럽 등 11개국 규제당국자 협의체로 우리나라는 2017년 12월에 가입했으며2021년에는 1년간 의장국을 맡아 수행했다. 식약처는 IMDRF 정회원으로서 동 국제 공통 가이드라인 마련을 위한 작업반에 적극 참여하고 있다. 식약처 관계자는 “소프트웨어 등디지털의료기기의 증가와 함께 사이버보안에대한위협도 증가하고 있다"며 "이번 가이드라인이 의료기기 사이버 위협으로부터 환자 안전을 확보하는데 도움을 줄 것으로 기대한다”고 전했다. 이어 “앞으로도 급변하는 디지털 환경에 신속히 대응하고 더욱 안전한 의료기기의 개발과 사용을 지원하기 위한 정보를 지속적으로 제공할 예정”이라고 덧붙였다. 자세한 내용은 ‘식약처 대표 누리집(mfds.go.kr)→법령/자료→법령정보→민원인안내서’에서 확인할 수 있다. -
![[기획-디지털 ID 기술] ㊿ 티보솔루션, '시간 기반 메타 데이터 검색 기준에 기초하여 멀티미디어 콘텐츠의 타겟된 세그먼트를 보기 위한 사용자 인터페이스' 명칭의 미국 특허 등록 (US 11709888)](http://stdnews.kr/data/file/news/thumb/thumb-3555376243_1Ouy0tRn_7e8b31bd407e08696497e73e1276bb227bc9dbcc_200x180.jpg) [기획-디지털 ID 기술] ㊿ 티보솔루션, '시간 기반 메타 데이터 검색 기준에 기초하여 멀티미디어 콘텐츠의 타겟된 세그먼트를 보기 위한 사용자 인터페이스' 명칭의 미국 특허 등록 (US 11709888)미국 엔터테인먼트 기술 기업 티보솔루션(TIVO SOLUTIONS)에 따르면 2023년 7월25일 '시간 기반 메타 데이터 검색 기준에 기초하여 멀티미디어 콘텐츠의 타겟된 세그먼트를 보기 위한 사용자 인터페이스(User interface for viewing targeted segments of multimedia content based on time-based metadata search criteria)' 명칭의 미국 특허(US 11709888)가 등록됐다.본 등록 특허(US 11709888)는 모출원 등록 특허(US 10372758)를 기초로 2019년 6월19일 계속 출원(US 16/446448)되어 미국 특허청에 의해 심사를 받았다.모출원 등록 특허(US 10372758)는 2011년 12월22일 출원(US 13/334285)되어 2019년 8월6일 등록(US 10372758)됐다. 패밀리 특허로 미국 특허(US 2023/0325437)가 2023년 5월 25일 출원되어 심사 중이다.본 등록 특허(US 11709888)는 사용자 입력에 응답해 검색 쿼리를 수신하고 처리하도록 구성된 네비게이션 시스템을 포함하는 디지털 미디어 자산을 탐색하기 위한 시스템 및 방법에 관한 특허다.본 등록 특허의 일 실시예에 따르면 디지털 미디어 자산의 기존 메타데이터와 시간 기반 메타데이터의 검색 인덱스에 검색 쿼리를 적용하고, 검색 쿼리를 만족하는 디지털 미디어 자산의 제목과 시작 시점에 대한 검색 결과를 결정한다. 내비게이션 시스템은 사용자 인터페이스를 통해 검색 결과를 사용자에게 표시할 수 있다. 검색 결과는 계층적 형식으로 표시될 수 있다.디지털 미디어 자산의 제목이 표시되고 디지털 미디어 자산의 제목을 선택하면 해당 디지털 미디어 자산 내의 시작 지점이 사용자 인터페이스를 통해 사용자에게 비디오로 표시되거나 재생된다.
[기획-디지털 ID 기술] ㊿ 티보솔루션, '시간 기반 메타 데이터 검색 기준에 기초하여 멀티미디어 콘텐츠의 타겟된 세그먼트를 보기 위한 사용자 인터페이스' 명칭의 미국 특허 등록 (US 11709888)미국 엔터테인먼트 기술 기업 티보솔루션(TIVO SOLUTIONS)에 따르면 2023년 7월25일 '시간 기반 메타 데이터 검색 기준에 기초하여 멀티미디어 콘텐츠의 타겟된 세그먼트를 보기 위한 사용자 인터페이스(User interface for viewing targeted segments of multimedia content based on time-based metadata search criteria)' 명칭의 미국 특허(US 11709888)가 등록됐다.본 등록 특허(US 11709888)는 모출원 등록 특허(US 10372758)를 기초로 2019년 6월19일 계속 출원(US 16/446448)되어 미국 특허청에 의해 심사를 받았다.모출원 등록 특허(US 10372758)는 2011년 12월22일 출원(US 13/334285)되어 2019년 8월6일 등록(US 10372758)됐다. 패밀리 특허로 미국 특허(US 2023/0325437)가 2023년 5월 25일 출원되어 심사 중이다.본 등록 특허(US 11709888)는 사용자 입력에 응답해 검색 쿼리를 수신하고 처리하도록 구성된 네비게이션 시스템을 포함하는 디지털 미디어 자산을 탐색하기 위한 시스템 및 방법에 관한 특허다.본 등록 특허의 일 실시예에 따르면 디지털 미디어 자산의 기존 메타데이터와 시간 기반 메타데이터의 검색 인덱스에 검색 쿼리를 적용하고, 검색 쿼리를 만족하는 디지털 미디어 자산의 제목과 시작 시점에 대한 검색 결과를 결정한다. 내비게이션 시스템은 사용자 인터페이스를 통해 검색 결과를 사용자에게 표시할 수 있다. 검색 결과는 계층적 형식으로 표시될 수 있다.디지털 미디어 자산의 제목이 표시되고 디지털 미디어 자산의 제목을 선택하면 해당 디지털 미디어 자산 내의 시작 지점이 사용자 인터페이스를 통해 사용자에게 비디오로 표시되거나 재생된다. -
![[미국] 스트린트스펙트럼과 프리즘테크놀로지의 특허 무효 시 손해 배상](http://stdnews.kr/data/file/news/thumb/thumb-3555377333_G9WjMXgz_e341e7aeaa5dfe9463908de3bce29a2318be7dcc_200x180.jpg) [미국] 스트린트스펙트럼과 프리즘테크놀로지의 특허 무효 시 손해 배상2016년 스위스 다보스포럼에서 클라우스 슈밥이 '제4차 산업혁명'이라는 용어를 처음 사용한 이후 4년이 흘렀다. 이러한 4차 산업혁명의 시대는 초기술 융합의 시대라고 부른다.예를 들어 4차산업의 대표적인 분야인 드론의 경우에 첨단소재, 배터리, 카메라, 운영체제(OS) 등 첨단기술 집약체이다. 특히 인공지능(AI), 로봇, 자율주행 자동차, 빅데이터, 블록체인과 융·복합적으로 관련돼 있다.이와 같은 초기술 융합의 시대에서는 특허권의 확보를 통한 특허경영이 기업의 미래뿐만 아니라 국가의 미래를 결정할 수도 있다. 또한 유효한 특허권을 적절히 확보해 외부의 공격으로부터 방어하는 것 역시 더욱 더 중요해지고 있다.아래에 제시된 판례는 스프린트스펙트럼(Sprint Spectrum)과 프리즘테크놀로지(Prism Technology) 간의 특허권의 무효에 따른 영향을 보여준다.국문요약: 스프린트스펙트럼이 프리즘테크놀로지에 대한 $US 3200만불의 손해 배상 책임 판결을 받았다. 하지만 아직 집행되지 않은 상태에서, 이후에 T-모바일이 프리즘테크놀로지의 특허를 무효화시켰다.이에 따라 스프린트스펙트럼은 이전 판결에 대한 구제를 요청해 지방법원은 스프린트스펙트럼의 요청을 받아들였다. 프리즘테크놀로지는 이에 대해 항소했으며 연방순회항소법원은 지방법원의 판결이 적절했다고 판결했다. 영문요약: Effect on Damages when Patent Is Invalidated Prism Tech. v. Sprint Spectrum L.P. (F.C. 2019)Case History:•Sprint was liable for $32M damage, which was affirmed in March 2017 by FC.•Prism had another litigation with T-Mobile.•T-Mobile challenged the eligibility of the patents under S101 and won.•On June 2017, FC affirmed the invalidation of the Prism’s patent at issue. FC Decision:•FC ruled in favor of Sprint.•After the invalidation of the patent, Sprint filed a motion for Relief from Judgment based on FC’s decision on invalidation.•District court agreed and FC found no abuse of discretion.Key Point:•Sprint was able to avoid paying $32M in damages due to T-Mobile’s effort to invalidate Prism’s patent.•Sprint took as much time as possible to stick around and see how the case between Prism and T-Mobile would turn out, and that turned out beneficial to Sprint.•There was a strong federal patent policy against enforcing an unexecuted judgment of the patent liability when the patent claims underlying that judgment had been held invalid by another decision.
[미국] 스트린트스펙트럼과 프리즘테크놀로지의 특허 무효 시 손해 배상2016년 스위스 다보스포럼에서 클라우스 슈밥이 '제4차 산업혁명'이라는 용어를 처음 사용한 이후 4년이 흘렀다. 이러한 4차 산업혁명의 시대는 초기술 융합의 시대라고 부른다.예를 들어 4차산업의 대표적인 분야인 드론의 경우에 첨단소재, 배터리, 카메라, 운영체제(OS) 등 첨단기술 집약체이다. 특히 인공지능(AI), 로봇, 자율주행 자동차, 빅데이터, 블록체인과 융·복합적으로 관련돼 있다.이와 같은 초기술 융합의 시대에서는 특허권의 확보를 통한 특허경영이 기업의 미래뿐만 아니라 국가의 미래를 결정할 수도 있다. 또한 유효한 특허권을 적절히 확보해 외부의 공격으로부터 방어하는 것 역시 더욱 더 중요해지고 있다.아래에 제시된 판례는 스프린트스펙트럼(Sprint Spectrum)과 프리즘테크놀로지(Prism Technology) 간의 특허권의 무효에 따른 영향을 보여준다.국문요약: 스프린트스펙트럼이 프리즘테크놀로지에 대한 $US 3200만불의 손해 배상 책임 판결을 받았다. 하지만 아직 집행되지 않은 상태에서, 이후에 T-모바일이 프리즘테크놀로지의 특허를 무효화시켰다.이에 따라 스프린트스펙트럼은 이전 판결에 대한 구제를 요청해 지방법원은 스프린트스펙트럼의 요청을 받아들였다. 프리즘테크놀로지는 이에 대해 항소했으며 연방순회항소법원은 지방법원의 판결이 적절했다고 판결했다. 영문요약: Effect on Damages when Patent Is Invalidated Prism Tech. v. Sprint Spectrum L.P. (F.C. 2019)Case History:•Sprint was liable for $32M damage, which was affirmed in March 2017 by FC.•Prism had another litigation with T-Mobile.•T-Mobile challenged the eligibility of the patents under S101 and won.•On June 2017, FC affirmed the invalidation of the Prism’s patent at issue. FC Decision:•FC ruled in favor of Sprint.•After the invalidation of the patent, Sprint filed a motion for Relief from Judgment based on FC’s decision on invalidation.•District court agreed and FC found no abuse of discretion.Key Point:•Sprint was able to avoid paying $32M in damages due to T-Mobile’s effort to invalidate Prism’s patent.•Sprint took as much time as possible to stick around and see how the case between Prism and T-Mobile would turn out, and that turned out beneficial to Sprint.•There was a strong federal patent policy against enforcing an unexecuted judgment of the patent liability when the patent claims underlying that judgment had been held invalid by another decision. -
 식약처, 나트륨·당류 저감 식품 개발 적극 지원식품의약품안전처는 국민의 건강한 식생활에 도움을 주기 위해 나트륨·당류 저감 제품 개발 기술지원 사업을 추진한 결과 나트륨·당류를 줄인 김밥 등 가공식품 11종과 치킨 등 조리식품 7종이 시장에 출시됐다고 23일 밝혔다. 나트륨·당류 저감 제품 생산 활성화로 국민의 건강한 식생활이 조성될 것으로 기대된다. 현재 우리나라 국민의 나트륨 섭취량은 3,080mg(2021년 기준)으로 세계보건기구(WHO) 권고기준(2,000mg)보다 1.5배 높은 수준이며 당류의 경우 여자 청소년 등 일부 연령층에서 권고기준이상으로 당류를 섭취하고 있어 식약처는 나트륨·당류 저감화 정책을 꾸준히 추진해 오고 있다. 식약처는 이번 사업에 참여한 중소 식품제조·가공업체와 식품접객업소 영업자에게 나트륨·당류 저감화 방법을 제공하고 전문가와 소비자를 대상으로 선호도 조사를 실시해 총 18종의 제품 개발을 지원했다. 이번에 개발된 제품은 양념육이나 소스 등과 같이 나트륨 함량이 높은 재료는 줄이고 채소 등으로 대체하거나 설탕의 사용을 줄인대신 당알콜 등을 사용해 시중에 유통되는 제품보다 나트륨·당류의 함량을 10% 이상 줄였다. 아울러 개발된 식품에는 지난 10월 개정된 ‘나트륨·당류 저감 표시기준’에 따라 ‘덜 짠’, ‘당류를 줄인’등 저감 제품임을 표시할 수 있다. 식약처는 향후저감 표시기준에 대한 영업자의 이해를 돕기 위해 ‘나트륨·당류 저감 표시기준 가이드라인’을 배포할 계획이다. 식약처 관계자는 “앞으로도 나트륨·당류 저감 제품의 개발을 적극적으로 지원하고 생산·유통을 활성화해 국민의 건강한 식생활 환경을 조성하기 위해 최선을 다할 것”이라고 전했다.
식약처, 나트륨·당류 저감 식품 개발 적극 지원식품의약품안전처는 국민의 건강한 식생활에 도움을 주기 위해 나트륨·당류 저감 제품 개발 기술지원 사업을 추진한 결과 나트륨·당류를 줄인 김밥 등 가공식품 11종과 치킨 등 조리식품 7종이 시장에 출시됐다고 23일 밝혔다. 나트륨·당류 저감 제품 생산 활성화로 국민의 건강한 식생활이 조성될 것으로 기대된다. 현재 우리나라 국민의 나트륨 섭취량은 3,080mg(2021년 기준)으로 세계보건기구(WHO) 권고기준(2,000mg)보다 1.5배 높은 수준이며 당류의 경우 여자 청소년 등 일부 연령층에서 권고기준이상으로 당류를 섭취하고 있어 식약처는 나트륨·당류 저감화 정책을 꾸준히 추진해 오고 있다. 식약처는 이번 사업에 참여한 중소 식품제조·가공업체와 식품접객업소 영업자에게 나트륨·당류 저감화 방법을 제공하고 전문가와 소비자를 대상으로 선호도 조사를 실시해 총 18종의 제품 개발을 지원했다. 이번에 개발된 제품은 양념육이나 소스 등과 같이 나트륨 함량이 높은 재료는 줄이고 채소 등으로 대체하거나 설탕의 사용을 줄인대신 당알콜 등을 사용해 시중에 유통되는 제품보다 나트륨·당류의 함량을 10% 이상 줄였다. 아울러 개발된 식품에는 지난 10월 개정된 ‘나트륨·당류 저감 표시기준’에 따라 ‘덜 짠’, ‘당류를 줄인’등 저감 제품임을 표시할 수 있다. 식약처는 향후저감 표시기준에 대한 영업자의 이해를 돕기 위해 ‘나트륨·당류 저감 표시기준 가이드라인’을 배포할 계획이다. 식약처 관계자는 “앞으로도 나트륨·당류 저감 제품의 개발을 적극적으로 지원하고 생산·유통을 활성화해 국민의 건강한 식생활 환경을 조성하기 위해 최선을 다할 것”이라고 전했다. -
 식약처, ‘범부처 의료기기 제품화 지원 거버넌스 통합포럼’ 개최식품의약품안전처가 의료기기 제품화 지원을 위한 포럼을 개최한다. 포럼에서 의료기기 분야별 제품화 지원사례와 성과를 공유하고 연구자 맞춤형 상담을 제공할 계획이다. 식약처는 범부처전주기의료기기연구개발사업단과 함께 연구자와 협력기관간 만남의 장을 마련하고 의료기기 제품화 전략을 안내하기 23일‘2023년 범부처 의료기기 제품화 지원 거버넌스 통합포럼’을 서울드래곤시티 컨벤션에서 개최한다고 밝혔다. 협력기관은대구첨단의료산업진흥재단, 오송첨단의료산업진흥재단, 한국화학융합시험연구원, 고려대학교 구로병원 등범부처 사업 내 식약처 지원사업 참여 17개 기관이다. 이번 통합포럼에서는 의료기기 규제과학 마일스톤을 활용한 제품화 전략에 대해 안내하고의료기기 분야별제품화 지원사례와 성과를 공유하며 연구자와 협력기관 간 1:1 맞춤형 상담을 제공한다. 의료기기 규제과학 마일스톤은 의료기기 개발 시 허가에 필요한 자료 준비를 스스로 확인·점검하는 자가점검표를 말한다. 식약처 관계자는 “앞으로도 규제과학 전문성을 기반으로 국내 의료기기 연구·개발 시발생할 수 있는 시행착오를 줄이고신속하게 제품을 개발하는 데 도움을 주기 위해 최선을 다해 지원하겠다”고 전했다.
식약처, ‘범부처 의료기기 제품화 지원 거버넌스 통합포럼’ 개최식품의약품안전처가 의료기기 제품화 지원을 위한 포럼을 개최한다. 포럼에서 의료기기 분야별 제품화 지원사례와 성과를 공유하고 연구자 맞춤형 상담을 제공할 계획이다. 식약처는 범부처전주기의료기기연구개발사업단과 함께 연구자와 협력기관간 만남의 장을 마련하고 의료기기 제품화 전략을 안내하기 23일‘2023년 범부처 의료기기 제품화 지원 거버넌스 통합포럼’을 서울드래곤시티 컨벤션에서 개최한다고 밝혔다. 협력기관은대구첨단의료산업진흥재단, 오송첨단의료산업진흥재단, 한국화학융합시험연구원, 고려대학교 구로병원 등범부처 사업 내 식약처 지원사업 참여 17개 기관이다. 이번 통합포럼에서는 의료기기 규제과학 마일스톤을 활용한 제품화 전략에 대해 안내하고의료기기 분야별제품화 지원사례와 성과를 공유하며 연구자와 협력기관 간 1:1 맞춤형 상담을 제공한다. 의료기기 규제과학 마일스톤은 의료기기 개발 시 허가에 필요한 자료 준비를 스스로 확인·점검하는 자가점검표를 말한다. 식약처 관계자는 “앞으로도 규제과학 전문성을 기반으로 국내 의료기기 연구·개발 시발생할 수 있는 시행착오를 줄이고신속하게 제품을 개발하는 데 도움을 주기 위해 최선을 다해 지원하겠다”고 전했다. -
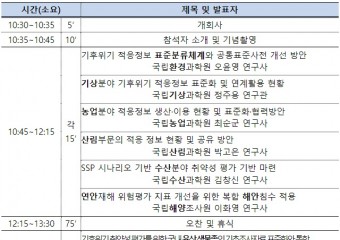
 식약처, ‘생물학적제제 품질관리실험실 네트워크(Lab-Net) 워크숍’ 개최식품의약품안전처는 백신·혈장분획제제 품질관리에 대한 최신 기술정보를 공유하는 ‘2023년 생물학적제제 품질관리실험실 네트워크(Lab-Net) 워크숍’을 23일 오송 C&V센터에서 개최한다고 밝혔다. 이번 워크숍으로 백신·혈장분획제제 업계의 품질관리 역량을 강화하는 데 도움이 될 것으로 기대된다. ‘생물학적제제 품질관리실험실 네트워크(Lab-Net)’는 식약처와 백신·혈장분획제제 제조·수입업체, 품질 검사기관 등이 참여하는 민·관 협의체로 2011년에 출범한 이후 품질관리 분야에서 활발하게 교류하며 국내 백신, 혈장분획제제 품질을 높이는 데 기여해 왔다. 이번 워크숍은 전문가 강연과 2023년 Lab-Net 운영 현황 및 내년도 계획 등에 대한 발표로 구성돼 있다. 전문가 초청 강연에서는 ▲시험방법 밸리데이션을 위한 통계 방법 ▲미국약전 생물학적 정량법 밸리데이션 ▲데이터 완전성과 컴퓨터 시스템 밸리데이션 ▲오염 관리 전략 수립 접근방법 등을 소개한다. 아울러 ▲백신 역가 시험법 개선 ▲항트롬빈III제제국가표준품 확립공동연구 ▲혈장분획제제 동물대체시험법 추진 등 Lab-Net 운영 성과와 내년도 계획에 대해서도 안내한다. 식약처 관계자는 “이번 워크숍이 백신·혈장분획제제 업계의 품질관리 역량을 강화하는 데 도움을 줄 것으로 기대한다”며 “앞으로도 전문성과 규제과학에 기반한 철저한 품질관리를 수행하여 안전한 제품이 국민께 공급될 수 있도록 최선을 다해 노력할 계획”이라고 밝혔다.
식약처, ‘생물학적제제 품질관리실험실 네트워크(Lab-Net) 워크숍’ 개최식품의약품안전처는 백신·혈장분획제제 품질관리에 대한 최신 기술정보를 공유하는 ‘2023년 생물학적제제 품질관리실험실 네트워크(Lab-Net) 워크숍’을 23일 오송 C&V센터에서 개최한다고 밝혔다. 이번 워크숍으로 백신·혈장분획제제 업계의 품질관리 역량을 강화하는 데 도움이 될 것으로 기대된다. ‘생물학적제제 품질관리실험실 네트워크(Lab-Net)’는 식약처와 백신·혈장분획제제 제조·수입업체, 품질 검사기관 등이 참여하는 민·관 협의체로 2011년에 출범한 이후 품질관리 분야에서 활발하게 교류하며 국내 백신, 혈장분획제제 품질을 높이는 데 기여해 왔다. 이번 워크숍은 전문가 강연과 2023년 Lab-Net 운영 현황 및 내년도 계획 등에 대한 발표로 구성돼 있다. 전문가 초청 강연에서는 ▲시험방법 밸리데이션을 위한 통계 방법 ▲미국약전 생물학적 정량법 밸리데이션 ▲데이터 완전성과 컴퓨터 시스템 밸리데이션 ▲오염 관리 전략 수립 접근방법 등을 소개한다. 아울러 ▲백신 역가 시험법 개선 ▲항트롬빈III제제국가표준품 확립공동연구 ▲혈장분획제제 동물대체시험법 추진 등 Lab-Net 운영 성과와 내년도 계획에 대해서도 안내한다. 식약처 관계자는 “이번 워크숍이 백신·혈장분획제제 업계의 품질관리 역량을 강화하는 데 도움을 줄 것으로 기대한다”며 “앞으로도 전문성과 규제과학에 기반한 철저한 품질관리를 수행하여 안전한 제품이 국민께 공급될 수 있도록 최선을 다해 노력할 계획”이라고 밝혔다.




![[특집-기술위원회] TC 229 나노기술(Nanotechnologies)... 나노기술 분야 표준화](http://stdnews.kr/data/file/news/thumb/thumb-32068165_FpALlyRW_23bfade8877a50180ae7aaab7c0adf74a8a562b9_340x240.jpg)
![[특집-기술위원회] TC 228 관광 및 관련 서비스(Tourism and related services)... 관광서비스 제](http://stdnews.kr/theme/wide03/img/default/no_img.gif)
![[특집-기술위원회] TC 226 1차 알루미늄 생산용 재료(Materials for the production of prima](http://stdnews.kr/data/file/news/thumb/thumb-32068165_ob2OKngD_470b16302d4df0fe99cfe7584a5ca27811606441_340x240.jpg)
![[특집-기술위원회] TC 227 스프링(Springs)](http://stdnews.kr/data/file/news/thumb/thumb-3698770111_x3sdiZe2_fc4f9a5c2b487b9cb1cfb2ba5d32e16d0c2733c0_340x240.jpg)

![[일본] 요코하마(横浜), 3월 원격근무로 일하는 50대 여성이 장시간 노동을 강요받아 적응장애가 발병해 산재로 인정받아](http://stdnews.kr/data/file/news/thumb/thumb-3555377672_BapV2SmF_41a011a26290be1daa3f6a5220df7b8b6d167f69_340x240.jpg)
![[인도] 마하라슈트라주 식품의약국(Maharashtra FDA), 맥도날드 상품명에 치즈를 잘못 표기해 소비자 기만 지적](http://stdnews.kr/data/file/news/thumb/thumb-3743818281_Uu5GpcKZ_6890f33f4b087f58686ed20e46a04bbb79ad883e_340x240.jpg)
![[남아공] 토코만 푸드(Thokoman Foods), 자사 땅콩버터 식품 안전성 재확인](http://stdnews.kr/data/file/news/thumb/thumb-3743818281_h5HrK0kT_c2453abdb4577a16b34590f5b8f76de9c2a95469_340x240.jpg)
![[남아공] 사기방지서비스(SAFPS), 고용 애플리케이션 활용 사기 전년 대비 106% 급증](http://stdnews.kr/data/file/news/thumb/thumb-32068165_vhbwMfDO_d466509ecb0542e9be7cc74ba85e9122e65195c9_340x240.jpg)

![[일본] 정부, 전국 약 1800개의 지방자치단체가 사용하는 정보기술(IT) 시스템을 공통화할 계획](http://stdnews.kr/data/file/news/thumb/thumb-32068165_k57HcuaC_ec1c1c40ab22bacb5547865a845790615e059a71_340x240.jpg)
![[일본] 소비자청(消費者庁), 5월 중 기능성 표시 식품 관련 제도를 전면 재검토할 계획](http://stdnews.kr/data/file/news/thumb/thumb-3698770111_kxPwWpEb_40955dfb17799431ea435609be9619c5595c5eac_340x240.jpg)
![[특집-기상기후재난] 한국중부발전(주) 신정철 선임 인터뷰 - 행정안전부 뿐 아니라 기상기후 연계조직 모두가 참여하는 협의체가](http://stdnews.kr/data/file/news/thumb/thumb-3555374516_iKWwUBas_9c1729f1e3977ee50c398986e7f98d5002a57deb_340x240.jpg)
![[특집-기상기후재난] (주)비밍코어 정성민 대표 인터뷰 - 인공지능(AI) 활용한 기후재난 대처 솔루션 개발](http://stdnews.kr/data/file/news/thumb/thumb-3555374391_0JZYhIcj_dca23c54fc7923952082a9d7af92db00b9dd33c9_340x240.jpg)
![[기획-표준 전문가] 한국투자증권 김범수 FC 인터뷰 - 표준전문가 양성 교육이 지속되길 희망](http://stdnews.kr/data/file/news/thumb/thumb-3555374114_Np9hM7aC_e6ffa916aade15e1c301badf3132ed3f0551a900_340x240.jpg)
![[특집-기상기후재난] 행정안전부 안전교육 전문인력 유정희 강사 인터뷰 - 기상기후재난예방 전문가 양성 시급](http://stdnews.kr/data/file/news/thumb/thumb-3555374240_gOmdLG10_cfc17ed887dccc93f503013bf794ed568a5d40dc_340x240.jpg)
![[특집-기상기후재난] (주)이토스 김형식 대표 인터뷰 - 재난을 사전에 예측·예방할 기술개발 시급](http://stdnews.kr/data/file/news/thumb/thumb-32068165_lmUrCBIn_797dc8926bb7d90542546463cc73e6233f0bbb46_340x240.png)