검색결과
-
 산자부, 5월 중 총 228개 도전‧혁신적인 과제 2차 공고 예정산업통상자원부(장관 안덕근, 이하 산자부)에 따르면 5월 중 총 228개의 도전‧혁신적인 과제를 2차로 공고해 신속하게 지원하기로 했다. 2차로 공고될 과제는 모빌리티 분야, 에너지 분야, 바이오 분야, 반도체 분야, 로봇 분야 등이다. 모빌리티 분야는 △비‧안개 등 악천후에서도 정확하게 볼 수 있는 자율주행 센서‧카메라 △96%이상 하이니켈계 이차전지 △메탄올 추진선 엔진 핵심부품 개발 등이 포함됐다. 에너지분야에는 △기존 실리콘 기반 태양전지의 효율 한계를 뛰어 넘는 탠덤 차세대 태양전지 △세계최초 수소 인프라 연계 수소전소 터빈 발전시스템(50~100MW) △액체수소 운반선 저장탱크용 진공단열시스템 개발 등을 지원한다. 바이오 분야에는 △주사제 아닌 먹는 암치료 항체의약품 △심혈관 질환을 예측‧진단하는 웨어러블 기기 개발 등이다. 반도체 분야에는 △데이터 취득이 어려운 제조 환경에 적합한 스몰 학습데이터 기반 온디바이스 AI 품질 검사 최적화 기술개발 등을 추진한다. 로봇 분야에서는 △피부일체형 로봇핸드 △인공지능 초미세(직경 0.8mm이하) 수술로봇 등을 개발한다. 산자부는 금년 1~3월 프로그램형 연구개발(R&D)사업 1차 공고를 통해 세계 최초·최고수준의 기술개발에 도전하는 총 700여개 과제를 선정한 바 있다. 1차 공고 지원과제 중 ‘전기차용 고전압 GaN 전력모듈 기술개발’ 과제에는 세미파워렉스(주관)와 함께 현대차, 삼성전자, 서울대학교 등이 컨소시엄을 구성하여 참여했다. 1.2kV 초고전압 전력반도체 상용화 개발의 도전적 목표를 정부가 제시하자 국내 최고 대·중소기업과 대학이 드림팀을 구성해 참여하는 등 혁신형 정부 R&D 사업이 국내 최고 연구자와 기업들의 협력을 촉진하고 있다. 전기차용 초고전압 GaN 전력반도체뿐 아니라 △주사제 아닌 먹는 암치료 항체의약품 △96%이상 하이니켈 이차전지 △탠덤 차세대 태양전지 △수소전소 터빈 발전시스템 등 도전혁신형 기술개발이 산자부 프로그램형 연구개발(R&D) 사업으로 추진된다. 참고로 산자부 프로그램형 사업(총 24개)은 자동차, 에너지, 전자부품 등 산업별 환경 변화와 현장 연구수요에 신속하게 대응하기 위해 예산심사시 규모만 확정하고 연구과제는 부처가 자율 기획하는 사업이다. 산자부 오승철 산업기반실장은 “산업부는 프로그램형 사업을 통해 급격한 산업환경의 변화와 기업 수요에 대응해 투자의 적시성과 유연성을 높이고, 도전적인 기술개발 목표 제시를 통해 정부 연구개발(R&D)의 파급력을 높여나갈 것”이라고 밝혔다.
산자부, 5월 중 총 228개 도전‧혁신적인 과제 2차 공고 예정산업통상자원부(장관 안덕근, 이하 산자부)에 따르면 5월 중 총 228개의 도전‧혁신적인 과제를 2차로 공고해 신속하게 지원하기로 했다. 2차로 공고될 과제는 모빌리티 분야, 에너지 분야, 바이오 분야, 반도체 분야, 로봇 분야 등이다. 모빌리티 분야는 △비‧안개 등 악천후에서도 정확하게 볼 수 있는 자율주행 센서‧카메라 △96%이상 하이니켈계 이차전지 △메탄올 추진선 엔진 핵심부품 개발 등이 포함됐다. 에너지분야에는 △기존 실리콘 기반 태양전지의 효율 한계를 뛰어 넘는 탠덤 차세대 태양전지 △세계최초 수소 인프라 연계 수소전소 터빈 발전시스템(50~100MW) △액체수소 운반선 저장탱크용 진공단열시스템 개발 등을 지원한다. 바이오 분야에는 △주사제 아닌 먹는 암치료 항체의약품 △심혈관 질환을 예측‧진단하는 웨어러블 기기 개발 등이다. 반도체 분야에는 △데이터 취득이 어려운 제조 환경에 적합한 스몰 학습데이터 기반 온디바이스 AI 품질 검사 최적화 기술개발 등을 추진한다. 로봇 분야에서는 △피부일체형 로봇핸드 △인공지능 초미세(직경 0.8mm이하) 수술로봇 등을 개발한다. 산자부는 금년 1~3월 프로그램형 연구개발(R&D)사업 1차 공고를 통해 세계 최초·최고수준의 기술개발에 도전하는 총 700여개 과제를 선정한 바 있다. 1차 공고 지원과제 중 ‘전기차용 고전압 GaN 전력모듈 기술개발’ 과제에는 세미파워렉스(주관)와 함께 현대차, 삼성전자, 서울대학교 등이 컨소시엄을 구성하여 참여했다. 1.2kV 초고전압 전력반도체 상용화 개발의 도전적 목표를 정부가 제시하자 국내 최고 대·중소기업과 대학이 드림팀을 구성해 참여하는 등 혁신형 정부 R&D 사업이 국내 최고 연구자와 기업들의 협력을 촉진하고 있다. 전기차용 초고전압 GaN 전력반도체뿐 아니라 △주사제 아닌 먹는 암치료 항체의약품 △96%이상 하이니켈 이차전지 △탠덤 차세대 태양전지 △수소전소 터빈 발전시스템 등 도전혁신형 기술개발이 산자부 프로그램형 연구개발(R&D) 사업으로 추진된다. 참고로 산자부 프로그램형 사업(총 24개)은 자동차, 에너지, 전자부품 등 산업별 환경 변화와 현장 연구수요에 신속하게 대응하기 위해 예산심사시 규모만 확정하고 연구과제는 부처가 자율 기획하는 사업이다. 산자부 오승철 산업기반실장은 “산업부는 프로그램형 사업을 통해 급격한 산업환경의 변화와 기업 수요에 대응해 투자의 적시성과 유연성을 높이고, 도전적인 기술개발 목표 제시를 통해 정부 연구개발(R&D)의 파급력을 높여나갈 것”이라고 밝혔다. -
![[기획 디지털 ID 정책] 5. 미국 개선신원연합(Better Identity Coalition)의 디지털 ID 정책](http://stdnews.kr/data/file/news/thumb/thumb-32068165_oyPYhCOQ_8c6c0cdbbec7ab27279ad1316777f0449ff51477_200x180.jpg) [기획 디지털 ID 정책] 5. 미국 개선신원연합(Better Identity Coalition)의 디지털 ID 정책미국 사이버보안 정책 및 법률센터(Center for Cybersecurity Policy & Law) 내 개선신원연합(Better Identity Coalition)은 2018년과 2022년 두차례에 걸쳐 디지털 신원증명(ID)에 관한 정책을 발표했다.첫 번째로 2018년 7월 연방 정책 입안자를 위한 청사진('Better Identity in America - A Blueprint for Policymakers')을 발표했다.연방 정책 입안자를 위한 청사진은 △차세대 원격 신원 증명 및 검증 시스템 개발 우선 △미국 사회보장번호 사용 방식 변경 △강력한 인증 촉진 및 우선순위 지정 △ID 시스템의 국제 조정 및 표준화 촉구 △더 나은 ID 솔루션에 대해 소비자와 기업을 교육 등 5가지 주요 이니셔티브를 포함하고 있다.두 번째로 개선신원연합은 2022년 12월 주정부 정책 입안자를 위한 청사진('Better Identity in America - A Blueprint for State Policymakers')을 발표했다.주정부 정책 입안자를 위한 청사진은 △주 디지털 신원 솔루션 센터에 DMV 배치 △차세대 소비자 중심의 원격 신원 증명 및 확인 시스템을 지원하기 위해 중요 기록국에서 속성 검증 서비스 구축 △더 나은 서비스를 위해 ID 혁신 수용 △ID가 모두에게 적합한지 확인 △강력한 인증 촉진 및 우선순위 지정 해를 끼치지 말 것(‘수술실에서와 마찬가지로’라는 모토 유지) 등 6가지 주요 이니셔티브를 포함하고 있다.개선신원연합이 발표한 연방 및 주 정책 입안자를 위한 청사진에 비영리단체인 사이버보안정책 및 법률센터(Center for Cybersecurity Policy and Law)의 프로젝트 연합이 참여하고 있다.또한 CVS, DISCOVER, EQUIFAX, Experian, facetec, Gen, ID.me, IDEMIA, incode, iproov, JpmorganChase&Co., LSEG, mastercard, Mircosoft, okta, PNC BANK, Qualcomm, TransUnion, usbank, WELLS FARGO, yubico, AT&T, Onfido 등 다수의 기업도 활동한다.참고로 사이버보안정책 및 법률센터는 501(c)(6)에 따라 2017년 설립된 비영리단체다. 정부, 민간 산업, 시민 사회에 보안 위협을 더 잘 관리하기 위한 관행과 정책을 제공해 전 세계적 사이버 보안을 강화하기 위해 활동한다.
[기획 디지털 ID 정책] 5. 미국 개선신원연합(Better Identity Coalition)의 디지털 ID 정책미국 사이버보안 정책 및 법률센터(Center for Cybersecurity Policy & Law) 내 개선신원연합(Better Identity Coalition)은 2018년과 2022년 두차례에 걸쳐 디지털 신원증명(ID)에 관한 정책을 발표했다.첫 번째로 2018년 7월 연방 정책 입안자를 위한 청사진('Better Identity in America - A Blueprint for Policymakers')을 발표했다.연방 정책 입안자를 위한 청사진은 △차세대 원격 신원 증명 및 검증 시스템 개발 우선 △미국 사회보장번호 사용 방식 변경 △강력한 인증 촉진 및 우선순위 지정 △ID 시스템의 국제 조정 및 표준화 촉구 △더 나은 ID 솔루션에 대해 소비자와 기업을 교육 등 5가지 주요 이니셔티브를 포함하고 있다.두 번째로 개선신원연합은 2022년 12월 주정부 정책 입안자를 위한 청사진('Better Identity in America - A Blueprint for State Policymakers')을 발표했다.주정부 정책 입안자를 위한 청사진은 △주 디지털 신원 솔루션 센터에 DMV 배치 △차세대 소비자 중심의 원격 신원 증명 및 확인 시스템을 지원하기 위해 중요 기록국에서 속성 검증 서비스 구축 △더 나은 서비스를 위해 ID 혁신 수용 △ID가 모두에게 적합한지 확인 △강력한 인증 촉진 및 우선순위 지정 해를 끼치지 말 것(‘수술실에서와 마찬가지로’라는 모토 유지) 등 6가지 주요 이니셔티브를 포함하고 있다.개선신원연합이 발표한 연방 및 주 정책 입안자를 위한 청사진에 비영리단체인 사이버보안정책 및 법률센터(Center for Cybersecurity Policy and Law)의 프로젝트 연합이 참여하고 있다.또한 CVS, DISCOVER, EQUIFAX, Experian, facetec, Gen, ID.me, IDEMIA, incode, iproov, JpmorganChase&Co., LSEG, mastercard, Mircosoft, okta, PNC BANK, Qualcomm, TransUnion, usbank, WELLS FARGO, yubico, AT&T, Onfido 등 다수의 기업도 활동한다.참고로 사이버보안정책 및 법률센터는 501(c)(6)에 따라 2017년 설립된 비영리단체다. 정부, 민간 산업, 시민 사회에 보안 위협을 더 잘 관리하기 위한 관행과 정책을 제공해 전 세계적 사이버 보안을 강화하기 위해 활동한다. -
![[특집-기술위원회] TC 173 - 보조 용품(Assistive products)… 개인의 줄어든 능력을 보정하는데 도움을 주기 위한 보조 용품 및 관련 서비스](http://stdnews.kr/data/file/news/thumb/thumb-32068165_O1fdGa7n_b687da6fe742a7d85be32b208bcb1cf56e269295_200x180.jpg) [특집-기술위원회] TC 173 - 보조 용품(Assistive products)… 개인의 줄어든 능력을 보정하는데 도움을 주기 위한 보조 용품 및 관련 서비스스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~TC 67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~TC 107 △1963년 TC 108~TC 111 △1964년 TC 112~TC 115, TC 117 △1965년 TC 118 △1966년 TC 119~TC 122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146, TC 147, TC 148, TC 149, TC 150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~TC 161 △1975년 TC 162~TC 164 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 등도 포함된다.ISO/TC 173 보조 용품(Assistive products)과 관련된 기술위원회는 TC 171, TC 172와 마찬가지로 1978년 결성됐다. 사무국은 스웨덴 표준연구소(Swedish Institute for Standards, SIS)에서 맡고 있다.위원회는 조아킴 포크(Mr Joakim Falk)가 책임지고 있으며 현재 의장은 마리타 브런딘(Ms Marita Brundin)이며 임기는 2025년까지다. ISO 기술 프로그램 관리자는 마호 타카하시(Mme Maho Takahashi), ISO 편집 관리자는 발레리아 아가멤논(Ms Valeria Agamennone) 등으로 조사됐다.범위는 개인의 줄어든 능력을 보정하는데 도움을 주기 위한 보조 용품 및 관련 서비스 분야의 표준화다. 단 기타 기술위원회 및 시스템위원회에서 다루고 있는 보조용품들은 제외한다.교통 수단(ISO/TC 8, 20, 22), 건물 건축(ISO/TC 59), 가구(ISO/TC 136), 수술용 임플란트(ISO/TC 150), 보철물 및 교정 장치(ISO/TC 150)에 대한 접근 /TC 168), 광학 및 포토닉스(ISO/TC 172), 전기 안전(IEC/TC 62), 보청기(IEC/TC 29), ICT 기술(JTC 1) 및 인체공학에서 다루는 설계 원리(ISO/TC 159) 및 적극적 생활 지원(IEC SyCAAL) 등이 포함된다.현재 ISO/TC 173 사무국과 관련해 발행된 표준은 95개며 이 중 ISO/TC 173 사무국의 직접적인 책임 하에 발행된 표준은 24개다.ISO/TC 173 사무국과 관련해 개발 중인 표준은 22개며 ISO/TC 173 사무국의 직접적인 책임 하에 개발 중인 표준은 11개다. 참여하고 있는 회원은 26개국, 참관 회원은 29개국이다.□ ISO/TC 173 사무국의 직접적인 책임 하에 발행된 표준 24개 중 15개 목록▷ISO 10535:2021 Assistive products — Hoists for the transfer of persons — Requirements and test methods▷ISO 11199-1:2021 Assistive products for walking manipulated by both arms — Requirements and test methods — Part 1: Walking frames▷ISO 11199-2:2021 Assistive products for walking manipulated by both arms — Requirements and test methods — Part 2: Rollators▷ISO 11199-3:2005 Walking aids manipulated by both arms — Requirements and test methods — Part 3: Walking tables▷ISO 11334-1:2007 Assistive products for walking manipulated by one arm — Requirements and test methods — Part 1: Elbow crutches▷ISO 11334-4:1999 Walking aids manipulated by one arm — Requirements and test methods — Part 4: Walking sticks with three or more legs▷ISO/TR 11548-1:2001 Communication aids for blind persons — Identifiers, names and assignation to coded character sets for 8-dot Braille characters — Part 1: General guidelines for Braille identifiers and shift marks▷ISO/TR 11548-2:2001 Communication aids for blind persons — Identifiers, names and assignation to coded character sets for 8-dot Braille characters — Part 2: Latin alphabet based character sets▷ISO 17966:2016 Assistive products for personal hygiene that support users — Requirements and test methods▷ISO 19894:2019 Walking trolleys — Requirements and test methods▷ISO 20342-1:2022 Assistive products for tissue integrity when lying down — Part 1: General requirements▷ISO/TR 20342-7:2021 Assistive products for tissue integrity when lying down — Part 7: Foam properties, characteristics and performance▷ISO/TS 20342-10:2022 Assistive products for tissue integrity when lying down — Part 10: Guidance to cleaning, disinfecting and care of polyurethane APTI covers▷ISO 21801-1:2020 Cognitive accessibility — Part 1: General guidelines▷ISO 21801-2:2022 Cognitive accessibility — Part 2: Reporting□ ISO/TC 173 사무국의 직접적인 책임 하에 개발 중인 표준 11개 목록▷ISO 11199-2:2021/DAmd 1 Assistive products for walking manipulated by both arms — Requirements and test methods — Part 2: Rollators — Amendment 1: Eliminate brake requirements in 6.5 Structure requirements▷ISO/DIS 11334-4 Assistive products for walking, manipulated by one arm — Requirements and test methods — Part 4: Walking sticks with three or more legs▷ISO/CD 17966 Assistive products for toileting, bathing and showering — Requirements and test methods▷ISO/AWI TR 20342-2 Assistive products for tissue integrity when lying down — Part 2: Microclimate▷ISO/CD 20342-3 Assistive products for tissue integrity when lying down — Part 3: Strength and impact▷ISO/CD 20342-4 Assistive products for tissue integrity when lying down — Part 4: Durability▷ISO/DIS 20342-5 Assistive products for tissue integrity when lying down — Part 5: Resistance to cleaning and disinfection▷ISO/AWI 20342-6 Assistive products for tissue integrity when lying down — Part 6: Horizontal stiffness▷ISO/CD 20342-8 Assistive products for tissue integrity when lying down — Part 8: Pressure distribution▷IEC/DIS 80601-2-52 Medical electrical equipment — Part 2-52: Particular requirements for the basic safety and essential performance of medical beds▷IEC/DIS 80601-2-89 Medical electrical equipment — Part 2-89: Particular requirements for the basic safety and essential performance of medical beds for children□ ISO/TC 173 사무국 분과위원회(Subcommittee)의 책임 하에 발행 및 개발 중인 표준 현황▷ISO/TC 173/SC 1 Wheelchairs ; 발행된 표준 41개, 개발 중인 표준 6개▷ISO/TC 173/SC 2 Classification and terminology ; 발행된 표준 1개, 개발 중인 표준 0개▷ISO/TC 173/SC 3 Aids for ostomy and incontinence ; 발행된 표준 23개, 개발 중인 표준 4개▷ISO/TC 173/SC 7 Assistive products for persons with impaired sensory functions ; 발행된 표준 6개, 개발 중인 표준 1개
[특집-기술위원회] TC 173 - 보조 용품(Assistive products)… 개인의 줄어든 능력을 보정하는데 도움을 주기 위한 보조 용품 및 관련 서비스스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~TC 67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~TC 107 △1963년 TC 108~TC 111 △1964년 TC 112~TC 115, TC 117 △1965년 TC 118 △1966년 TC 119~TC 122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146, TC 147, TC 148, TC 149, TC 150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~TC 161 △1975년 TC 162~TC 164 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 등도 포함된다.ISO/TC 173 보조 용품(Assistive products)과 관련된 기술위원회는 TC 171, TC 172와 마찬가지로 1978년 결성됐다. 사무국은 스웨덴 표준연구소(Swedish Institute for Standards, SIS)에서 맡고 있다.위원회는 조아킴 포크(Mr Joakim Falk)가 책임지고 있으며 현재 의장은 마리타 브런딘(Ms Marita Brundin)이며 임기는 2025년까지다. ISO 기술 프로그램 관리자는 마호 타카하시(Mme Maho Takahashi), ISO 편집 관리자는 발레리아 아가멤논(Ms Valeria Agamennone) 등으로 조사됐다.범위는 개인의 줄어든 능력을 보정하는데 도움을 주기 위한 보조 용품 및 관련 서비스 분야의 표준화다. 단 기타 기술위원회 및 시스템위원회에서 다루고 있는 보조용품들은 제외한다.교통 수단(ISO/TC 8, 20, 22), 건물 건축(ISO/TC 59), 가구(ISO/TC 136), 수술용 임플란트(ISO/TC 150), 보철물 및 교정 장치(ISO/TC 150)에 대한 접근 /TC 168), 광학 및 포토닉스(ISO/TC 172), 전기 안전(IEC/TC 62), 보청기(IEC/TC 29), ICT 기술(JTC 1) 및 인체공학에서 다루는 설계 원리(ISO/TC 159) 및 적극적 생활 지원(IEC SyCAAL) 등이 포함된다.현재 ISO/TC 173 사무국과 관련해 발행된 표준은 95개며 이 중 ISO/TC 173 사무국의 직접적인 책임 하에 발행된 표준은 24개다.ISO/TC 173 사무국과 관련해 개발 중인 표준은 22개며 ISO/TC 173 사무국의 직접적인 책임 하에 개발 중인 표준은 11개다. 참여하고 있는 회원은 26개국, 참관 회원은 29개국이다.□ ISO/TC 173 사무국의 직접적인 책임 하에 발행된 표준 24개 중 15개 목록▷ISO 10535:2021 Assistive products — Hoists for the transfer of persons — Requirements and test methods▷ISO 11199-1:2021 Assistive products for walking manipulated by both arms — Requirements and test methods — Part 1: Walking frames▷ISO 11199-2:2021 Assistive products for walking manipulated by both arms — Requirements and test methods — Part 2: Rollators▷ISO 11199-3:2005 Walking aids manipulated by both arms — Requirements and test methods — Part 3: Walking tables▷ISO 11334-1:2007 Assistive products for walking manipulated by one arm — Requirements and test methods — Part 1: Elbow crutches▷ISO 11334-4:1999 Walking aids manipulated by one arm — Requirements and test methods — Part 4: Walking sticks with three or more legs▷ISO/TR 11548-1:2001 Communication aids for blind persons — Identifiers, names and assignation to coded character sets for 8-dot Braille characters — Part 1: General guidelines for Braille identifiers and shift marks▷ISO/TR 11548-2:2001 Communication aids for blind persons — Identifiers, names and assignation to coded character sets for 8-dot Braille characters — Part 2: Latin alphabet based character sets▷ISO 17966:2016 Assistive products for personal hygiene that support users — Requirements and test methods▷ISO 19894:2019 Walking trolleys — Requirements and test methods▷ISO 20342-1:2022 Assistive products for tissue integrity when lying down — Part 1: General requirements▷ISO/TR 20342-7:2021 Assistive products for tissue integrity when lying down — Part 7: Foam properties, characteristics and performance▷ISO/TS 20342-10:2022 Assistive products for tissue integrity when lying down — Part 10: Guidance to cleaning, disinfecting and care of polyurethane APTI covers▷ISO 21801-1:2020 Cognitive accessibility — Part 1: General guidelines▷ISO 21801-2:2022 Cognitive accessibility — Part 2: Reporting□ ISO/TC 173 사무국의 직접적인 책임 하에 개발 중인 표준 11개 목록▷ISO 11199-2:2021/DAmd 1 Assistive products for walking manipulated by both arms — Requirements and test methods — Part 2: Rollators — Amendment 1: Eliminate brake requirements in 6.5 Structure requirements▷ISO/DIS 11334-4 Assistive products for walking, manipulated by one arm — Requirements and test methods — Part 4: Walking sticks with three or more legs▷ISO/CD 17966 Assistive products for toileting, bathing and showering — Requirements and test methods▷ISO/AWI TR 20342-2 Assistive products for tissue integrity when lying down — Part 2: Microclimate▷ISO/CD 20342-3 Assistive products for tissue integrity when lying down — Part 3: Strength and impact▷ISO/CD 20342-4 Assistive products for tissue integrity when lying down — Part 4: Durability▷ISO/DIS 20342-5 Assistive products for tissue integrity when lying down — Part 5: Resistance to cleaning and disinfection▷ISO/AWI 20342-6 Assistive products for tissue integrity when lying down — Part 6: Horizontal stiffness▷ISO/CD 20342-8 Assistive products for tissue integrity when lying down — Part 8: Pressure distribution▷IEC/DIS 80601-2-52 Medical electrical equipment — Part 2-52: Particular requirements for the basic safety and essential performance of medical beds▷IEC/DIS 80601-2-89 Medical electrical equipment — Part 2-89: Particular requirements for the basic safety and essential performance of medical beds for children□ ISO/TC 173 사무국 분과위원회(Subcommittee)의 책임 하에 발행 및 개발 중인 표준 현황▷ISO/TC 173/SC 1 Wheelchairs ; 발행된 표준 41개, 개발 중인 표준 6개▷ISO/TC 173/SC 2 Classification and terminology ; 발행된 표준 1개, 개발 중인 표준 0개▷ISO/TC 173/SC 3 Aids for ostomy and incontinence ; 발행된 표준 23개, 개발 중인 표준 4개▷ISO/TC 173/SC 7 Assistive products for persons with impaired sensory functions ; 발행된 표준 6개, 개발 중인 표준 1개 -
![[특집-기술위원회] TC 170 - 수술도구(Surgical instruments)… 겸자·가위·메스·리액터(견인기)](http://stdnews.kr/data/file/news/thumb/thumb-32068165_jTtlFPVH_d8130e2a1b743a90836718f61f95b966ec8092dc_200x180.jpg) [특집-기술위원회] TC 170 - 수술도구(Surgical instruments)… 겸자·가위·메스·리액터(견인기)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~TC 67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.△1962년 TC 105~TC 107 △1963년 TC 108~TC 111 △1964년 TC 112~TC 115, TC 117 △1965년 TC 118 △1966년 TC 119~TC 122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146, TC 147, TC 148, TC 149, TC 150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~TC 161 △1975년 TC 162~TC 164 △1976년 TC 165, TC 166 등도 포함된다.ISO/TC 170 수술도구(Surgical instruments)와 관련된 기술위원회는 TC 167, TC 168과 마찬가지로 1977년 결성됐다. 사무국은 독일 표준화기구(Deutsches Institut für Normung e.V., DIN)에서 맡고 있다.위원회는 페트라 비쇼프(Mrs Dipl.-Ing. (FH) Petra Bischoff)가 책임지고 있으며 현재 의장은 토드 포프(Mr Todd Pope)다. ISO 기술 프로그램 관리자는 페트리샤 쿡(Mme Patricia Cook), ISO 편집 관리자는 발레리아 아가멤논(Ms Valeria Agamennone) 등으로 조사됐다.범위는 겸자, 가위, 메스, 리액터(견인기)와 같은 수술 도구 분야의 표준화다. 단, ISO / TC 106 - 치과(Dentistry), ISO / TC 150 - 수술용임플란트(Implants for surgery)에서 다루고 있는 특수 도구는 제외한다.현재 ISO/TC 170 사무국의 직접적인 책임 하에 발행된 표준은 5개며 ISO/TC 170 사무국의 직접적인 책임 하에 개발 중인 표준은 7개다. 참여하고 있는 회원은 9개국, 참관 회원은 24개국이다.□ ISO/TC 170 사무국의 직접적인 책임 하에 발행된 표준 5개 목록▷ISO 7151:1988 Surgical instruments — Non-cutting, articulated instruments — General requirements and test methods▷ISO 7153-1:2016 Surgical instruments — Materials — Part 1: Metals▷ISO 7740:1985 Instruments for surgery — Scalpels with detachable blades — Fitting dimensions▷ISO 7741:1986 Instruments for surgery — Scissors and shears — General requirements and test methods▷ISO 13402:1995 Surgical and dental hand instruments — Determination of resistance against autoclaving, corrosion and thermal exposure□ ISO/TC 170 사무국의 직접적인 책임 하에 개발 중인 표준 7개 목록▷ISO/CD 6335-1 Surgical instruments — Staplers — Part 1: Vocabulary▷ISO/CD 6335-2 Surgical instruments — Staplers — Part 2: General requirements▷ISO/FDIS 7151 Surgical instruments — Non-cutting, articulated instruments — General requirements and test methods▷ISO/CD 7554-1 Surgical instruments — Terms, measuring methods and tests — Part 1: Vocabulary▷ISO/CD 7554-2 Surgical instruments — Terms, measuring methods and tests — Part 2: Measuring methods for the determination of basic measures of surgical standard instruments▷ISO/CD 7554-3 Surgical instruments -Terms, measuring methods and tests — Part 3: Test methods▷ISO/DIS 13402 Surgical and dental hand instruments — Determination of resistance against autoclaving, corrosion and thermal exposure
[특집-기술위원회] TC 170 - 수술도구(Surgical instruments)… 겸자·가위·메스·리액터(견인기)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~TC 67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.△1962년 TC 105~TC 107 △1963년 TC 108~TC 111 △1964년 TC 112~TC 115, TC 117 △1965년 TC 118 △1966년 TC 119~TC 122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146, TC 147, TC 148, TC 149, TC 150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~TC 161 △1975년 TC 162~TC 164 △1976년 TC 165, TC 166 등도 포함된다.ISO/TC 170 수술도구(Surgical instruments)와 관련된 기술위원회는 TC 167, TC 168과 마찬가지로 1977년 결성됐다. 사무국은 독일 표준화기구(Deutsches Institut für Normung e.V., DIN)에서 맡고 있다.위원회는 페트라 비쇼프(Mrs Dipl.-Ing. (FH) Petra Bischoff)가 책임지고 있으며 현재 의장은 토드 포프(Mr Todd Pope)다. ISO 기술 프로그램 관리자는 페트리샤 쿡(Mme Patricia Cook), ISO 편집 관리자는 발레리아 아가멤논(Ms Valeria Agamennone) 등으로 조사됐다.범위는 겸자, 가위, 메스, 리액터(견인기)와 같은 수술 도구 분야의 표준화다. 단, ISO / TC 106 - 치과(Dentistry), ISO / TC 150 - 수술용임플란트(Implants for surgery)에서 다루고 있는 특수 도구는 제외한다.현재 ISO/TC 170 사무국의 직접적인 책임 하에 발행된 표준은 5개며 ISO/TC 170 사무국의 직접적인 책임 하에 개발 중인 표준은 7개다. 참여하고 있는 회원은 9개국, 참관 회원은 24개국이다.□ ISO/TC 170 사무국의 직접적인 책임 하에 발행된 표준 5개 목록▷ISO 7151:1988 Surgical instruments — Non-cutting, articulated instruments — General requirements and test methods▷ISO 7153-1:2016 Surgical instruments — Materials — Part 1: Metals▷ISO 7740:1985 Instruments for surgery — Scalpels with detachable blades — Fitting dimensions▷ISO 7741:1986 Instruments for surgery — Scissors and shears — General requirements and test methods▷ISO 13402:1995 Surgical and dental hand instruments — Determination of resistance against autoclaving, corrosion and thermal exposure□ ISO/TC 170 사무국의 직접적인 책임 하에 개발 중인 표준 7개 목록▷ISO/CD 6335-1 Surgical instruments — Staplers — Part 1: Vocabulary▷ISO/CD 6335-2 Surgical instruments — Staplers — Part 2: General requirements▷ISO/FDIS 7151 Surgical instruments — Non-cutting, articulated instruments — General requirements and test methods▷ISO/CD 7554-1 Surgical instruments — Terms, measuring methods and tests — Part 1: Vocabulary▷ISO/CD 7554-2 Surgical instruments — Terms, measuring methods and tests — Part 2: Measuring methods for the determination of basic measures of surgical standard instruments▷ISO/CD 7554-3 Surgical instruments -Terms, measuring methods and tests — Part 3: Test methods▷ISO/DIS 13402 Surgical and dental hand instruments — Determination of resistance against autoclaving, corrosion and thermal exposure -
![[특집-기술위원회] TC 150 - 수술용 임플란트(Implants for surgery)](http://stdnews.kr/data/file/news/thumb/thumb-3555378151_I5n9NHAu_c200214d4172f6cc368e1125b329b7b4dbfb2438_200x180.jpg) [특집-기술위원회] TC 150 - 수술용 임플란트(Implants for surgery)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~TC 67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 등이다.△1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104, △1962년 TC 105~TC 107, △1963년 TC 108~TC 111, △1964년 TC 112~TC 115, TC 117, △1965년 TC 118, △1966년 TC 119~TC 122, △1967년 TC 123, △1968년 TC 126, TC 127, △1969년 TC 130~136, △1970년 TC 137, TC 138, TC 142, TC 145 등도 포함된다.ISO/TC 150 수술용 임플란트(Implants for surgery)와 관련된 기술위원회는 TC 146, TC 147, TC 148, TC 149과 마찬가지로 1971년 결성됐다. 사무국은 독일 표준화기구(Deutsches Institut für Normung e.V., DIN)에서 맡고 있다.위원회는 클라우스 자이어(Mr Klaus Zeier)가 책임지고 있다. 현재 의장은 하니 데미안(Mr Hany Demian)으로 임기는 2025년까지다.ISO 기술 프로그램 관리자는 페트리샤 쿡(Mme Patricia Cook), ISO 편집 관리자는 산잘리 자인(Ms Sanjali Jain) 등으로 조사됐다.범위는 수술용 임플란트 분야의 표준화다. 또한 수술용 임플란트에 필요한 장비의 표준화뿐아니라 모든 유형의 임플란트, 제조 및 적용에 사용되는 기본 및 복합 재료에 대한 용어, 사양, 테스트 방법을 다루고 있다.수술용 임플란트는 진단 또는 치료 목적으로 일시적 또는 영구적으로 신체에 외과적으로 이식되는 물체 또는 장치를 말한다.현재 ISO/TC 150 사무국과 관련해 발행된 표준은 170개며 이 중 사무국의 직접적인 책임 하에 발행된 표준은 17개다. SO/TC 150 사무국과 관련해 개발중인 표준은 51개며 이 중 직접적인 책임 하에 개발 중인 표준은 4개다. 참여하고 있는 회원은 24개국, 참관 회원은 22개국이다.□ ISO/TC 150 사무국의 직접적인 책임 하에 발행된 표준 17개 목록▷ISO 7197:2006 Neurosurgical implants — Sterile, single-use hydrocephalus shunts and components▷ISO 7197:2006/Cor 1:2007 Neurosurgical implants — Sterile, single-use hydrocephalus shunts and components — Technical Corrigendum 1▷ISO 9713:2022 Neurosurgical implants — Self-closing intracranial aneurysm clips▷ISO 12891-1:2015 Retrieval and analysis of surgical implants — Part 1: Retrieval and handling▷ISO 12891-2:2020 Retrieval and analysis of surgical implants — Part 2: Analysis of retrieved surgical implants▷ISO 13179-1:2021 Implants for surgery — Coatings on metallic surgical implants — Part 1: Plasma-sprayed coatings derived from titanium or titanium-6 aluminum-4 vanadium alloy powders▷ISO/TR 14283:2018 Implants for surgery — Essential principles of safety and performance▷ISO 14607:2018 Non-active surgical implants — Mammary implants — Particular requirements▷ISO 14630:2012 Non-active surgical implants — General requirements▷ISO 16054:2019 Implants for surgery — Minimum data sets for surgical implants▷ISO 16061:2021 Instruments for use in association with non-active surgical implants — General requirements▷ISO 17327-1:2018 Non-active surgical implants — Implant coating — Part 1: General requirements▷ISO/TR 17327-2:2021 Non-active surgical implants — Implant coating — Part 2: Reference standards related to coatings▷ISO 19213:2017 Implants for surgery — Test methods of material for use as a cortical bone model▷ISO 19227:2018 Implants for surgery — Cleanliness of orthopedic implants — General requirements▷ISO/TS 20721:2020 Implants for surgery — General guidelines and requirements for assessment of absorbable metallic implants▷ISO 22926:2023 Implants for surgery — Specification and verification of synthetic anatomical bone models for testing □ ISO/TC 150 사무국의 직접적인 책임 하에 개발 중인 표준 4개 목록▷ISO/CD 5092 Additive manufacturing for medical — General principles — Additive manufacturing of non-active implants ▷ISO/DIS 7197 Neurosurgical implants — Sterile, single-use hydrocephalus shunts▷ISO/DIS 14607 Non-active surgical implants — Mammary implants — Specific requirements▷ISO/FDIS 14630 Non-active surgical implants — General requirements□ ISO/TC 150 사무국 분과위원회(Subcommittee)의 책임 하에 발행 및 개발 중인 표준 현황▷ISO/TC 150/SC 1 Materials ; 발행된 표준 38개, 개발 중인 표준 13개▷ISO/TC 150/SC 2 Cardiovascular implants and extracorporeal systems ; 발행된 표준 37개, 개발 중인 표준 15개▷ISO/TC 150/SC 4 Bone and joint replacements ; 발행된 표준 36개, 개발 중인 표준 12개▷ISO/TC 150/SC 5 Osteosynthesis and spinal devices ; 발행된 표준 26개, 개발 중인 표준 1개▷ISO/TC 150/SC 6 Active implants ; 발행된 표준 16개, 개발 중인 표준 4개▷ISO/TC 150/SC 7 Tissue-engineered medical products ; 발행된 표준 5개, 개발 중인 표준 2개
[특집-기술위원회] TC 150 - 수술용 임플란트(Implants for surgery)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~TC 67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 등이다.△1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104, △1962년 TC 105~TC 107, △1963년 TC 108~TC 111, △1964년 TC 112~TC 115, TC 117, △1965년 TC 118, △1966년 TC 119~TC 122, △1967년 TC 123, △1968년 TC 126, TC 127, △1969년 TC 130~136, △1970년 TC 137, TC 138, TC 142, TC 145 등도 포함된다.ISO/TC 150 수술용 임플란트(Implants for surgery)와 관련된 기술위원회는 TC 146, TC 147, TC 148, TC 149과 마찬가지로 1971년 결성됐다. 사무국은 독일 표준화기구(Deutsches Institut für Normung e.V., DIN)에서 맡고 있다.위원회는 클라우스 자이어(Mr Klaus Zeier)가 책임지고 있다. 현재 의장은 하니 데미안(Mr Hany Demian)으로 임기는 2025년까지다.ISO 기술 프로그램 관리자는 페트리샤 쿡(Mme Patricia Cook), ISO 편집 관리자는 산잘리 자인(Ms Sanjali Jain) 등으로 조사됐다.범위는 수술용 임플란트 분야의 표준화다. 또한 수술용 임플란트에 필요한 장비의 표준화뿐아니라 모든 유형의 임플란트, 제조 및 적용에 사용되는 기본 및 복합 재료에 대한 용어, 사양, 테스트 방법을 다루고 있다.수술용 임플란트는 진단 또는 치료 목적으로 일시적 또는 영구적으로 신체에 외과적으로 이식되는 물체 또는 장치를 말한다.현재 ISO/TC 150 사무국과 관련해 발행된 표준은 170개며 이 중 사무국의 직접적인 책임 하에 발행된 표준은 17개다. SO/TC 150 사무국과 관련해 개발중인 표준은 51개며 이 중 직접적인 책임 하에 개발 중인 표준은 4개다. 참여하고 있는 회원은 24개국, 참관 회원은 22개국이다.□ ISO/TC 150 사무국의 직접적인 책임 하에 발행된 표준 17개 목록▷ISO 7197:2006 Neurosurgical implants — Sterile, single-use hydrocephalus shunts and components▷ISO 7197:2006/Cor 1:2007 Neurosurgical implants — Sterile, single-use hydrocephalus shunts and components — Technical Corrigendum 1▷ISO 9713:2022 Neurosurgical implants — Self-closing intracranial aneurysm clips▷ISO 12891-1:2015 Retrieval and analysis of surgical implants — Part 1: Retrieval and handling▷ISO 12891-2:2020 Retrieval and analysis of surgical implants — Part 2: Analysis of retrieved surgical implants▷ISO 13179-1:2021 Implants for surgery — Coatings on metallic surgical implants — Part 1: Plasma-sprayed coatings derived from titanium or titanium-6 aluminum-4 vanadium alloy powders▷ISO/TR 14283:2018 Implants for surgery — Essential principles of safety and performance▷ISO 14607:2018 Non-active surgical implants — Mammary implants — Particular requirements▷ISO 14630:2012 Non-active surgical implants — General requirements▷ISO 16054:2019 Implants for surgery — Minimum data sets for surgical implants▷ISO 16061:2021 Instruments for use in association with non-active surgical implants — General requirements▷ISO 17327-1:2018 Non-active surgical implants — Implant coating — Part 1: General requirements▷ISO/TR 17327-2:2021 Non-active surgical implants — Implant coating — Part 2: Reference standards related to coatings▷ISO 19213:2017 Implants for surgery — Test methods of material for use as a cortical bone model▷ISO 19227:2018 Implants for surgery — Cleanliness of orthopedic implants — General requirements▷ISO/TS 20721:2020 Implants for surgery — General guidelines and requirements for assessment of absorbable metallic implants▷ISO 22926:2023 Implants for surgery — Specification and verification of synthetic anatomical bone models for testing □ ISO/TC 150 사무국의 직접적인 책임 하에 개발 중인 표준 4개 목록▷ISO/CD 5092 Additive manufacturing for medical — General principles — Additive manufacturing of non-active implants ▷ISO/DIS 7197 Neurosurgical implants — Sterile, single-use hydrocephalus shunts▷ISO/DIS 14607 Non-active surgical implants — Mammary implants — Specific requirements▷ISO/FDIS 14630 Non-active surgical implants — General requirements□ ISO/TC 150 사무국 분과위원회(Subcommittee)의 책임 하에 발행 및 개발 중인 표준 현황▷ISO/TC 150/SC 1 Materials ; 발행된 표준 38개, 개발 중인 표준 13개▷ISO/TC 150/SC 2 Cardiovascular implants and extracorporeal systems ; 발행된 표준 37개, 개발 중인 표준 15개▷ISO/TC 150/SC 4 Bone and joint replacements ; 발행된 표준 36개, 개발 중인 표준 12개▷ISO/TC 150/SC 5 Osteosynthesis and spinal devices ; 발행된 표준 26개, 개발 중인 표준 1개▷ISO/TC 150/SC 6 Active implants ; 발행된 표준 16개, 개발 중인 표준 4개▷ISO/TC 150/SC 7 Tissue-engineered medical products ; 발행된 표준 5개, 개발 중인 표준 2개 -
디지털 트윈 기술의 발전과 표준을 통한 산업 가속화디지털 트윈은 1960년대 NASA에서 처음 개념을 도입한 이후 급속한 발전을 이루었다. 이는 우주선 사고 시 우주선의 디지털 모델을 생성하고 데이터로 공급하여 시뮬레이션을 통해 더 원활한 운용을 보장하는 기술로 시작되었다. 디지털 트윈은 현실 세계의 물리적 대상 등을 디지털적으로 모델링하여 현실 세계의 상태나 특징을 시뮬레이션하고 데이터를 수집 및 분석하는 기술이다. 현재에는 인공 지능과 사물 인터넷의 발전으로 디지털 트윈은 스마트 제조, 농업, 의료, 스마트 시티, 광업 등 다양한 분야에서 적용되고 있다. 디지털 트윈은 제품의 분석, 설계, 테스트에 활용되며, 도시 기획자는 도시를 재현하여 다양한 기반 시설이나 교통 수단을 실험할 수 있으며, 외과 의사는 실제 환자에 대한 수술 전 디지털 트윈 환자를 활용하여 연습할 수 있다. 디지털 트윈은 또한 운영 환경에서 모니터링과 예방 정비를 비롯한 다양한 목적으로 활용되며, 여러 디지털 트윈이 상호 연결되어 복잡한 시스템을 모델링하여 스마트 시티와 같은 복합 시스템을 지원한다. 그러나 디지털 트윈의 사용이 다양한 도메인에서 급증하면서 정의와 용어의 다양성이 증가하고, 이로 인해 업계에서는 상호 운용성과 의사 소통에 어려움이 발생하고 있다. 이에 대응하기 위해 IEC가 최근에 ISO/IEC 30173 표준을 출판하여 디지털 트윈과 관련된 일련의 업종 중립적인 용어와 정의를 제공하며, 다양한 이해 관계자 간의 의사 소통을 용이하게 하고 국제 및 교차 섹터 활동을 촉진하고 있다. 디지털 트윈에 대한 표준 개발을 통하여 일련의 중립적인 용어 및 정의가 사용되고 공통 기준을 갖는 것이 가능해질 것으로 보인다.
-
![[미국] 미국소아과학회(AAP), 신생아치료 수준에 대한 인력 등을 지정하는 새로운 표준 구현](http://stdnews.kr/data/file/news/thumb/thumb-3745424048_Z8q3LrXP_12b2468dcf3615ad9c763a6e47478a7396534887_200x180.jpg) [미국] 미국소아과학회(AAP), 신생아치료 수준에 대한 인력 등을 지정하는 새로운 표준 구현미국소아과학회(American Academy of Pediatrics, AAP)는 신생아 치료 수준에 필요한 인력, 장비, 기타 시비스를 지정하는 새로운 표준을 구현했다고 밝혔다.표준은 갓난아이를 위해 제공하는 병원에 대해 정의하고 있다. 이 표준은 특수 보육원(레벨 II)에서 수술을 포함한 복잡한 세부 전문 치료(레벨 IV)에 이르기까지 각 수준의 신생아 치료에 대한 최소한의 구성요소를 성문화했다.신생아 치료 레벨에 대한 표준 II, III, IV는 증거 기반 문헌 및 전문 실무 표준인 AAP 정책을 기반으로 한다. 시설이 가족 중심 치료에 중점을 두고 환자, 가족 및 지역사회의 의료 불균형을 평가하도록 장려한다.새로운 표준이 발표되고 프로세스가 마련되면 AAP 프로그램은 신생아 시설의 규정 준수 확인 및 특정 수준의 신생아 관리(II, III, IV)를 제공하도록 지정할 수 있다.지금까지 공중보건부와 같은 주별 지정 기관에서 직접 감독했다. AAP 프로그램은 특정 주에서 신생아 관리 수준에 대한 조사기관 역할만 수행했다.신생아 집중치료실(neonatal intensive care unit, NICU) 표준 발행은 AAP NICU 검증 프로그램을 전국적으로 확장하려는 노력이 시작됐음을 의미한다.모든 주에서 의료시설을 규제하지만 신생아 관리 수준 및 요구사항 준수에 대한 사양은 매우 다양하다. 현재 제3자 조사기관에 의해 검증을 요구하는 주는 거의 없다.국가 신생아 검증 프로그램은 고품질의 동등한 치료에 필수적이다. 전문가들은 시설을 신중하게 평가할 수 있는 숙련된 조사팀에 의한 정직한 평가를 받는 것이 중요하다고 주장한다.병원은 데이터를 제출하고 시설에 대한 설문조사를 받는다. 요구사항을 충족한다면 특정 수준의 신생아 치료를 위한 AAP 인증을 받았다고 볼 수 있다. Pediatrics 6월호(https://doi.org/10.1542/peds.2023-061957) 링크를 통해 관련 내용을 확인할 수 있다. 신생아 관리 수준 및 주산기 관리 매뉴얼 지침서인 제8판 AAP 정책 선언문을 함께 제공한다.
[미국] 미국소아과학회(AAP), 신생아치료 수준에 대한 인력 등을 지정하는 새로운 표준 구현미국소아과학회(American Academy of Pediatrics, AAP)는 신생아 치료 수준에 필요한 인력, 장비, 기타 시비스를 지정하는 새로운 표준을 구현했다고 밝혔다.표준은 갓난아이를 위해 제공하는 병원에 대해 정의하고 있다. 이 표준은 특수 보육원(레벨 II)에서 수술을 포함한 복잡한 세부 전문 치료(레벨 IV)에 이르기까지 각 수준의 신생아 치료에 대한 최소한의 구성요소를 성문화했다.신생아 치료 레벨에 대한 표준 II, III, IV는 증거 기반 문헌 및 전문 실무 표준인 AAP 정책을 기반으로 한다. 시설이 가족 중심 치료에 중점을 두고 환자, 가족 및 지역사회의 의료 불균형을 평가하도록 장려한다.새로운 표준이 발표되고 프로세스가 마련되면 AAP 프로그램은 신생아 시설의 규정 준수 확인 및 특정 수준의 신생아 관리(II, III, IV)를 제공하도록 지정할 수 있다.지금까지 공중보건부와 같은 주별 지정 기관에서 직접 감독했다. AAP 프로그램은 특정 주에서 신생아 관리 수준에 대한 조사기관 역할만 수행했다.신생아 집중치료실(neonatal intensive care unit, NICU) 표준 발행은 AAP NICU 검증 프로그램을 전국적으로 확장하려는 노력이 시작됐음을 의미한다.모든 주에서 의료시설을 규제하지만 신생아 관리 수준 및 요구사항 준수에 대한 사양은 매우 다양하다. 현재 제3자 조사기관에 의해 검증을 요구하는 주는 거의 없다.국가 신생아 검증 프로그램은 고품질의 동등한 치료에 필수적이다. 전문가들은 시설을 신중하게 평가할 수 있는 숙련된 조사팀에 의한 정직한 평가를 받는 것이 중요하다고 주장한다.병원은 데이터를 제출하고 시설에 대한 설문조사를 받는다. 요구사항을 충족한다면 특정 수준의 신생아 치료를 위한 AAP 인증을 받았다고 볼 수 있다. Pediatrics 6월호(https://doi.org/10.1542/peds.2023-061957) 링크를 통해 관련 내용을 확인할 수 있다. 신생아 관리 수준 및 주산기 관리 매뉴얼 지침서인 제8판 AAP 정책 선언문을 함께 제공한다. -
 의약품안전관리원, 의료용 용어 표준화 작업 박차한국의약품안전관리원은 의료기관별로 상이한 임상 용어를 표준화하는 기준을 마련하기 위해 전문위원들을 구성해 운영한다고 17일 밝혔다. 이에 '병원 자료 기반 공통데이터모델(MOA CDM)' 참여 의료기관 및 유관 학회 관계자 등 전문가 30명을 'MOA CDM 용어표준화위원회 전문위원'으로 위촉하고, 16일 위촉식을 개최했다. 이들의 임기는 2년이다. MOA CDM은 병원별로 다양한 전자의무기록 용어체계 및 자료형식을 CDM 형태로 표준화한 자료이며, 의약품안전원에서는 2022년까지 총 27개 의료기관의 약 3,300만 명 환자 정보를 CDM으로 구축해 의약품 안전정보 분석에 활용하고 있다. 이처럼 수많은 환자들의 정확한 의약품 안전정보 분석 결과를 얻기 위해서는 임상 용어의 표준화 기준에 대한 지속적인 점검과 논의가 필요하다. 이를 위해 용어표준화위원회에서는 기존에 구축된 CDM에서 약물, 검사, 진단 등 임상 용어를 표준화하는 기준을 마련하고 주요 이슈를 파악하여 개선안을 마련할 예정이다. 1기 위원회에서는 CDM 임상용어 중 약물, 진단 용어에 대한 표준화 방안을 중점적으로 논의했으며, 2기에서는 처치·수술, 검사 용어 표준화에 대한 논의가 주로 이뤄질 예정이다. 이를 위해 2기 전문위원은 CDM 참여 의료기관 및 유관 학회 추천 등을 통해 30인으로 확대하는 등 보다 다양한 분야의 전문가를 확충했다. 오정원 원장은 "제2기 용어표준화위원회 전문위원 위촉으로 신뢰성 높은 의약품 안전정보 생산을 위한 심도 있는 논의가 이루어지기를 기대한다"고 밝혔다.
의약품안전관리원, 의료용 용어 표준화 작업 박차한국의약품안전관리원은 의료기관별로 상이한 임상 용어를 표준화하는 기준을 마련하기 위해 전문위원들을 구성해 운영한다고 17일 밝혔다. 이에 '병원 자료 기반 공통데이터모델(MOA CDM)' 참여 의료기관 및 유관 학회 관계자 등 전문가 30명을 'MOA CDM 용어표준화위원회 전문위원'으로 위촉하고, 16일 위촉식을 개최했다. 이들의 임기는 2년이다. MOA CDM은 병원별로 다양한 전자의무기록 용어체계 및 자료형식을 CDM 형태로 표준화한 자료이며, 의약품안전원에서는 2022년까지 총 27개 의료기관의 약 3,300만 명 환자 정보를 CDM으로 구축해 의약품 안전정보 분석에 활용하고 있다. 이처럼 수많은 환자들의 정확한 의약품 안전정보 분석 결과를 얻기 위해서는 임상 용어의 표준화 기준에 대한 지속적인 점검과 논의가 필요하다. 이를 위해 용어표준화위원회에서는 기존에 구축된 CDM에서 약물, 검사, 진단 등 임상 용어를 표준화하는 기준을 마련하고 주요 이슈를 파악하여 개선안을 마련할 예정이다. 1기 위원회에서는 CDM 임상용어 중 약물, 진단 용어에 대한 표준화 방안을 중점적으로 논의했으며, 2기에서는 처치·수술, 검사 용어 표준화에 대한 논의가 주로 이뤄질 예정이다. 이를 위해 2기 전문위원은 CDM 참여 의료기관 및 유관 학회 추천 등을 통해 30인으로 확대하는 등 보다 다양한 분야의 전문가를 확충했다. 오정원 원장은 "제2기 용어표준화위원회 전문위원 위촉으로 신뢰성 높은 의약품 안전정보 생산을 위한 심도 있는 논의가 이루어지기를 기대한다"고 밝혔다. -
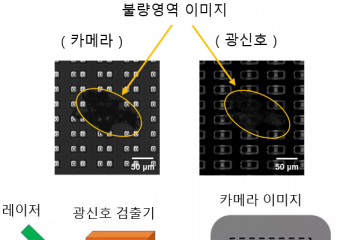
 국표원, 제1회 신기술·신제품 인증서 수여식 개최산업통상자원부 국가기술표준원은 17일 엘타워에서 ‘2023년 제1회 신기술(NET) 및 신제품(NEP) 인증서 수여식’을 개최하고 29개 혁신적인 신기술과 신제품에 대하여 인증서를 수여했다고 17일 밝혔다. NET과 NEP 인증은 국내에서 최초로 개발된 기술 또는 기존 기술을 혁신적으로 개선·개량한 우수 기술 및 이를 핵심으로 적용하여 상용화가 완료된 제품에 대해 평가하여 정부가 인증하는 제도다. NET 분야에서는 수술 시 뼈의 정렬을 정확하고 안전하게 교정하기 위한 수술로봇 기술 등 19개 신기술 개발기업이, NEP 분야에서는 전기자동차 배터리와 전장부품 등의 자동화 품질검사를 위한 고해상도 동영상 엑스레이 검출기 등 10개 신제품 개발기업이 인증서를 받게 됐다. 진종욱 국가기술표준원장은 “신기술·신제품 인증 기업들이 인증받은 기술과 제품을 통해 보다 적극적인 시장개척을 해 기업성장과 수출확대에 기여할 수 있기를 바란다”고 밝혔다.
국표원, 제1회 신기술·신제품 인증서 수여식 개최산업통상자원부 국가기술표준원은 17일 엘타워에서 ‘2023년 제1회 신기술(NET) 및 신제품(NEP) 인증서 수여식’을 개최하고 29개 혁신적인 신기술과 신제품에 대하여 인증서를 수여했다고 17일 밝혔다. NET과 NEP 인증은 국내에서 최초로 개발된 기술 또는 기존 기술을 혁신적으로 개선·개량한 우수 기술 및 이를 핵심으로 적용하여 상용화가 완료된 제품에 대해 평가하여 정부가 인증하는 제도다. NET 분야에서는 수술 시 뼈의 정렬을 정확하고 안전하게 교정하기 위한 수술로봇 기술 등 19개 신기술 개발기업이, NEP 분야에서는 전기자동차 배터리와 전장부품 등의 자동화 품질검사를 위한 고해상도 동영상 엑스레이 검출기 등 10개 신제품 개발기업이 인증서를 받게 됐다. 진종욱 국가기술표준원장은 “신기술·신제품 인증 기업들이 인증받은 기술과 제품을 통해 보다 적극적인 시장개척을 해 기업성장과 수출확대에 기여할 수 있기를 바란다”고 밝혔다. -
![[아랍에미리트] 보건부(MoHAP), 2023년말까지 스마트 디지털 의료 규제 프레임워크 도입 예정](http://stdnews.kr/data/file/news/thumb/thumb-1938433695_5bvqBlJU_8a00aeeed27b71cdbb57077ab708c5118fdfcc4f_200x180.jpg) [아랍에미리트] 보건부(MoHAP), 2023년말까지 스마트 디지털 의료 규제 프레임워크 도입 예정아랍에미리트(UAE) 보건부(Ministry of Health and Prevention, MoHAP)에 따르면 2023년말까지 스마트 디지털 의료 규제 프레임워크(Smart Digital Health regulatory framework)를 도입하기로 결정했다.지난 3월 보건부 산하 디지털의료부(Digital Health Department) 전략투자실(Strategy and Investment Section)은 두바이에서 개최된 원격포럼에서 도입 계획을 발표했다.UAE에서 도입되는 새로운 규제 프레임워크는 모든 의료 제공업자들이 환자를 위해 최소 하나의 원격 서비스 형태를 제공해야 될 의무를 부담하도록 했다.의료제공업자들은 컨설팅, 약물 처방, 환자 모니터링 또는 로봇 수술과 같은 이러한 서비스 중 적어도 하나를 원격으로 제공해야 된다. 새로운 규제는 공공 및 민간 영역의 의료 서비스 제공업자 모두에게 해당된다.의료 시설은 현재 운영하고 있는 가상 또는 원격 의료 서비스에 대해 보건부에 보고해야 된다. 만약 의료시설이 어떤 것도 보유하고 있지 않다면 올해 연말까지 원격 서비스 중 하나를 갖추도록 협력해 나갈 계획이다.모든 원격 의료 서비스를 규제하고 있는 포괄적인 의료 규제 프레임워크는 의료 시설 및 환자 권리에 대한 역할과 책임을 정의하고 있다.의료 분야의 기술 발전이 급속도로 발전함에 따라 의료 시설에서 원격 서비스를 촉진하는 것이 시급하기 때문이다.정부는 의료 관광으로 진화해 나가고 있는 상황에서 원격 의료 진료와 같은 기본 서비스가 필요하다고 판단했다. 또한 의료 부문 디지털화를 나아가기 위해서도 원격 의료 서비스 도입이 절실한 실정이다.보건부는 의료 진단 및 처방, 원격진료에 대한 의료적 책임이 필요하다고 보고 있으며 이를 위해 명확한 규정을 마련했다. 규칙과 규정을 통해 의료 서비스 제공자에게 경계를 명확히 설정할 수 있을 것으로 전망된다.
[아랍에미리트] 보건부(MoHAP), 2023년말까지 스마트 디지털 의료 규제 프레임워크 도입 예정아랍에미리트(UAE) 보건부(Ministry of Health and Prevention, MoHAP)에 따르면 2023년말까지 스마트 디지털 의료 규제 프레임워크(Smart Digital Health regulatory framework)를 도입하기로 결정했다.지난 3월 보건부 산하 디지털의료부(Digital Health Department) 전략투자실(Strategy and Investment Section)은 두바이에서 개최된 원격포럼에서 도입 계획을 발표했다.UAE에서 도입되는 새로운 규제 프레임워크는 모든 의료 제공업자들이 환자를 위해 최소 하나의 원격 서비스 형태를 제공해야 될 의무를 부담하도록 했다.의료제공업자들은 컨설팅, 약물 처방, 환자 모니터링 또는 로봇 수술과 같은 이러한 서비스 중 적어도 하나를 원격으로 제공해야 된다. 새로운 규제는 공공 및 민간 영역의 의료 서비스 제공업자 모두에게 해당된다.의료 시설은 현재 운영하고 있는 가상 또는 원격 의료 서비스에 대해 보건부에 보고해야 된다. 만약 의료시설이 어떤 것도 보유하고 있지 않다면 올해 연말까지 원격 서비스 중 하나를 갖추도록 협력해 나갈 계획이다.모든 원격 의료 서비스를 규제하고 있는 포괄적인 의료 규제 프레임워크는 의료 시설 및 환자 권리에 대한 역할과 책임을 정의하고 있다.의료 분야의 기술 발전이 급속도로 발전함에 따라 의료 시설에서 원격 서비스를 촉진하는 것이 시급하기 때문이다.정부는 의료 관광으로 진화해 나가고 있는 상황에서 원격 의료 진료와 같은 기본 서비스가 필요하다고 판단했다. 또한 의료 부문 디지털화를 나아가기 위해서도 원격 의료 서비스 도입이 절실한 실정이다.보건부는 의료 진단 및 처방, 원격진료에 대한 의료적 책임이 필요하다고 보고 있으며 이를 위해 명확한 규정을 마련했다. 규칙과 규정을 통해 의료 서비스 제공자에게 경계를 명확히 설정할 수 있을 것으로 전망된다.





![[특집-기술위원회] TC 229 나노기술(Nanotechnologies)... 나노기술 분야 표준화](http://stdnews.kr/data/file/news/thumb/thumb-32068165_FpALlyRW_23bfade8877a50180ae7aaab7c0adf74a8a562b9_340x240.jpg)
![[특집-기술위원회] TC 228 관광 및 관련 서비스(Tourism and related services)... 관광서비스 제](http://stdnews.kr/theme/wide03/img/default/no_img.gif)
![[특집-기술위원회] TC 226 1차 알루미늄 생산용 재료(Materials for the production of prima](http://stdnews.kr/data/file/news/thumb/thumb-32068165_ob2OKngD_470b16302d4df0fe99cfe7584a5ca27811606441_340x240.jpg)
![[특집-기술위원회] TC 227 스프링(Springs)](http://stdnews.kr/data/file/news/thumb/thumb-3698770111_x3sdiZe2_fc4f9a5c2b487b9cb1cfb2ba5d32e16d0c2733c0_340x240.jpg)


![[일본] 요코하마(横浜), 3월 원격근무로 일하는 50대 여성이 장시간 노동을 강요받아 적응장애가 발병해 산재로 인정받아](http://stdnews.kr/data/file/news/thumb/thumb-3555377672_BapV2SmF_41a011a26290be1daa3f6a5220df7b8b6d167f69_340x240.jpg)
![[인도] 마하라슈트라주 식품의약국(Maharashtra FDA), 맥도날드 상품명에 치즈를 잘못 표기해 소비자 기만 지적](http://stdnews.kr/data/file/news/thumb/thumb-3743818281_Uu5GpcKZ_6890f33f4b087f58686ed20e46a04bbb79ad883e_340x240.jpg)
![[남아공] 토코만 푸드(Thokoman Foods), 자사 땅콩버터 식품 안전성 재확인](http://stdnews.kr/data/file/news/thumb/thumb-3743818281_h5HrK0kT_c2453abdb4577a16b34590f5b8f76de9c2a95469_340x240.jpg)
![[남아공] 사기방지서비스(SAFPS), 고용 애플리케이션 활용 사기 전년 대비 106% 급증](http://stdnews.kr/data/file/news/thumb/thumb-32068165_vhbwMfDO_d466509ecb0542e9be7cc74ba85e9122e65195c9_340x240.jpg)

![[일본] 정부, 전국 약 1800개의 지방자치단체가 사용하는 정보기술(IT) 시스템을 공통화할 계획](http://stdnews.kr/data/file/news/thumb/thumb-32068165_k57HcuaC_ec1c1c40ab22bacb5547865a845790615e059a71_340x240.jpg)
![[일본] 소비자청(消費者庁), 5월 중 기능성 표시 식품 관련 제도를 전면 재검토할 계획](http://stdnews.kr/data/file/news/thumb/thumb-3698770111_kxPwWpEb_40955dfb17799431ea435609be9619c5595c5eac_340x240.jpg)
![[특집-기상기후재난] 한국중부발전(주) 신정철 선임 인터뷰 - 행정안전부 뿐 아니라 기상기후 연계조직 모두가 참여하는 협의체가](http://stdnews.kr/data/file/news/thumb/thumb-3555374516_iKWwUBas_9c1729f1e3977ee50c398986e7f98d5002a57deb_340x240.jpg)
![[특집-기상기후재난] (주)비밍코어 정성민 대표 인터뷰 - 인공지능(AI) 활용한 기후재난 대처 솔루션 개발](http://stdnews.kr/data/file/news/thumb/thumb-3555374391_0JZYhIcj_dca23c54fc7923952082a9d7af92db00b9dd33c9_340x240.jpg)
![[기획-표준 전문가] 한국투자증권 김범수 FC 인터뷰 - 표준전문가 양성 교육이 지속되길 희망](http://stdnews.kr/data/file/news/thumb/thumb-3555374114_Np9hM7aC_e6ffa916aade15e1c301badf3132ed3f0551a900_340x240.jpg)
![[특집-기상기후재난] 행정안전부 안전교육 전문인력 유정희 강사 인터뷰 - 기상기후재난예방 전문가 양성 시급](http://stdnews.kr/data/file/news/thumb/thumb-3555374240_gOmdLG10_cfc17ed887dccc93f503013bf794ed568a5d40dc_340x240.jpg)
![[특집-기상기후재난] (주)이토스 김형식 대표 인터뷰 - 재난을 사전에 예측·예방할 기술개발 시급](http://stdnews.kr/data/file/news/thumb/thumb-32068165_lmUrCBIn_797dc8926bb7d90542546463cc73e6233f0bbb46_340x240.png)